下列化学用语的表达正确的是
A.原子核内有10个中子的氧原子: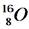 |
B.氯原子的结构示意图: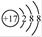 |
| C.Fe3+的最外层电子排布式为:3s23p63d5 |
D.基态铜原子的外围电子排布图: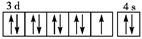 |
关于2mol二氧化碳的叙述中,正确的是( )
| A.质量为44g | B.有4mol原子 |
| C.分子数为6.02×1023 | D.摩尔质量为44g/mol |
摩尔是( )
| A.国际单位制的一个基本物理量 | B.表示物质质量的单位 |
| C.计量微观粒子的物质的量的单位 | D.表示6.02×1023个粒子的集体 |
下列说法正确的是( )
| A.1molO的质量是16g/mol | B.Na+ 的摩尔质量是23g/mol |
| C.CO2的摩尔质量是44 | D.氢的摩尔质量是2g/mol |
以色列科学家Daniel Shechtman因发现准晶体获得2011年诺贝尔化学奖。人们在自然界中也找到了组成为Al63Cu24Fe13的天然准晶体。将相同质量的此准晶体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为
| A.n(烧碱)<n(稀硝酸)<n(盐酸) | B.n(烧碱)<n(盐酸)<n(稀硝酸) |
| C.n(稀硝酸)<n(烧碱)<n(盐酸) | D.n(盐酸)<n(稀硝酸)<n(烧碱) |
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标况下,11.2 L HF所含的分子数目为0.5NA |
足量铜粉与一定量的浓硝酸充分反应,得到硝酸铜溶液和 NO2、N2O4、NO 的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好沉淀完全,则消耗 NaOH溶液的体积是( )
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
将9.0 g铜和铁的混合物投入100mL稀硝酸中,充分反应后得到标准状况下1.12L NO,剩余4.8 g金属;继续加入100mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下1.12L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法正确的是( )
| A.原混合物中铜和铁各0.075mol |
| B.稀硝酸的物质的量浓度为0.5mol·L-1 |
| C.第一次剩余4.8g金属为铜和铁 |
| D.再加入上述100mL稀硝酸,又得到标准状况下1.12L NO |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.7.8 gNa2S固体和7.8 gNa2O2固体中含有的阴离子数目均为0.1 NA |
| B.0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积约为2.24 L |
| D.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
NA表示阿伏加德罗常数的值,下列判断正确的是
| A.标准状况下,2.24 L16O2和3.6 g18O2均含有0.2NA个氧原子 |
| B.1.7 g H218O2中含有的电子数为0.9 NA |
| C.电解精炼铜时,若阴极得到NA个电子,则阳极质量减少32g |
| D.标准状况下,2.24 L甲烷、戊烷混合物所含分子数为0.1NA |