题目内容
关于2mol二氧化碳的叙述中,正确的是( )
| A.质量为44g | B.有4mol原子 |
| C.分子数为6.02×1023 | D.摩尔质量为44g/mol |
D
解析试题分析:A二氧化碳摩尔质量为44g/mol所以2mol二氧化碳质量为m=nM=2mol×44g/mol=88g.错误。B每个CO2分子中含有3个的原子,所以2mol二氧化碳含有6mol的原子。错误。C每mol二氧化碳中约含有分子数为6.02×1023,则2摩尔的二氧化碳中含有1.204×1024个分子。错误。D二氧化碳相对分子质量为44,它的摩尔质量也就是44g/mol.正确。
考点:考查阿伏伽德罗常数、质量、摩尔质量、物质的量、微粒数等的知识。

练习册系列答案
相关题目
下列物质含分子最多的是
| A.1.204×1024个O2 | B.3molCO2 |
| C.标准状况下89.6LCl2 | D.90g水 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是
A.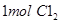 与足量Fe反应转移电子数一定为3NA 与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,22.4L NH3中含有共价键的数目为NA |
C.1.0L 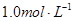 的 的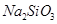 水溶液中含有的氧原子数为3NA 水溶液中含有的氧原子数为3NA |
D.4.6g Na完全转化成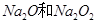 的混合物,混合物中阴离子总数为0.1NA 的混合物,混合物中阴离子总数为0.1NA |
用NA表示阿伏加德罗常数的值。下列判断错误的是( )
| A.NA个H+的质量为1 g |
| B.2 L 0.5mol/LNa2SO4溶液中含NA个Na+ |
| C.32 g O2中含有2NA个O原子 |
| D.标准状况下,1 mol H2O中含有NA个分子 |
足量铜粉与一定量的浓硝酸充分反应,得到硝酸铜溶液和 NO2、N2O4、NO 的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好沉淀完全,则消耗 NaOH溶液的体积是( )
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
将一定的 、
、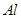 合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中
合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中 的物质的量( )
的物质的量( )
| A.0.01mol | B.0.02mol | C.0.03mol | D.0.04mol |
下列各溶液中,c( Na+ ) 最大的是( )
| A.4L 0.5mol/L的NaCl溶液 | B.2L 0.8mol/L的NaOH溶液 |
| C.1L 1mol/L的Na2CO3溶液 | D.0.5L 1.2mol/L的Na2SO4溶液 |
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是
| A.16g | B.32g | C.64g /mol | D.32g /mol |
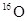 和
和 是氧元素的两种核素,
是氧元素的两种核素,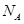 表示阿伏伽德罗常数,下列说法正确的是
表示阿伏伽德罗常数,下列说法正确的是
A.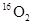 与 与 互为同分异构体 互为同分异构体 |
B.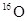 与 与 核外电子排布方式不同 核外电子排布方式不同 |
C.通过化学变化可以实现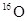 与 与 间的相互转化 间的相互转化 |
D.标准状况下,1.12L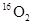 和1.12L 和1.12L 均含有0.1 均含有0.1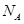 个氧原子 个氧原子 |