将钾与氧形成的化合物或混合物1.02 g溶于水后,可被0.25 mol/L 盐酸 80 mL恰好中和,则该物质的成分可能是
| A.K2O | B.K2O 和K2O2 | C.K2O2 | D.K2O2和KO2 |
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是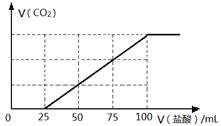
| A.原NaOH溶液的浓度为0.1 mol/L |
| B.通入CO2的体积为448 mL |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) =" 1:" 3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) =" 2:" 1 |
下列化学用语只能用来表示一种微粒的是
A. | B.2s22p6 | C.CH4O | D.C |
设NA为阿伏伽德罗常数的数值,则下列说法中,正确的是
A.常温下,0.1mol碳酸钠晶体中含有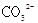 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下,11.2L苯含有C-H键数目为3NA |
| C.常温常压下,54 g重水(D2O)含水分子数为3NA |
| D.将NA个Cl2分子通入足量的水中,所转移的电子总数为NA |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.18g水中所含的电子数为8NA |
| B.11.2L氯气所含的分子数为0.5NA |
| C.2.4gMg与足量的盐酸反应失去的电子数为0.2NA |
| D.32g氧气中所含的氧原子数为NA |
NA为阿伏加德罗常数,下列说法正确的是
| A.标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B.28g乙烯所含共用电子对数目为4NA |
| C.1 mol甲基的电子数目为7NA |
| D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
下列说法正确的是(NA表示阿伏加德罗常数)
| A.1mol钠和足量水反应可生成11.2L氢气 |
| B.常温常压下,32g氧气中含有2NA个氧分子 |
| C.1mol/LK2SO4溶液中,含有2mol钾离子 |
| D.标准状况下,22.4LHCl溶于水后溶液中含有NA个氢离子 |
有Mg、Al、Fe、Cu四种金属,若两两混合,取混合物26g与足量稀硫酸反应,产生标准状况下H2 11.2L。此混合物的可能组成方式最多有
| A.2种 | B.3种 | C.4种 | D.5种 |
设阿伏加德罗常数为NA, 下列叙述中正确的是
| A.常温常压下, 32克氧气中原子个数为NA |
| B.标准状况下, 1mol H2O的体积为22.4L |
| C.常温常压下, 1molH2的质量为2克 |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |