下列化学用语正确的是
A.乙烯分子的电子式  |
B.硫原子的结构示意图 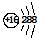 |
| C.淀粉的化学式 (C6H10O5)n |
| D.硫酸铁的电离方程式 Fe2(SO4)3 = 2Fe2+ + 3SO42ˉ |
相同条件下,质量相同的NH3和CH4,下列说法正确的是
| A.密度比为16:17 | B.氢原子比为3:4 |
| C.物质的量比为1:1 | D.体积比为16:17 |
已知标准状况下:①6.72L CH4 ②3.01×1023HCl ③23.1g CCl4 ④2.3g Na,下列对四种物质的
关系由小到大表示正确的是
| A.体积④<①<②<③ | B.密度①<④<③<② |
| C.原子数④<③<②<① | D.质量④<①<③<② |
若NA表示阿伏加德罗常数,下列说法中错误的是
| A.0.1mol/L稀硫酸中含有硫酸根离子个数为0.1NA |
| B.32g O2与O3混合气体中含有原子数为2NA |
| C.1molMg与足量N2反应生成Mg3N2失去的电子数为2NA |
| D.1mol H2和O2的混合气体在标准状况下的体积约为22.4L |
以下因素中,不会影响气体体积大小的是
| A.分子个数 | B.原子半径 | C.温度 | D.压强 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.标准状况下11.2 L NO和11.2 L O2混合后所得气体分子数为NA |
| B.7.1 g Cl2与足量的NaOH溶液反应转移的电子数为0.2NA |
| C.25℃、1.01×105 Pa时,80 g SO3中含有的原子数为4NA |
| D.NA个CO分子和0.5 mol CH4的质量比为7∶4 |
用NA表示阿佛加德罗常数,下列叙述中正确的是
| A.常温常压下,22.4 L的氧气含氧原子数为2NA |
| B.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA |
| C.常温下,23g NO2含有NA个氧原子 |
| D.足量铜与1L 18mol·L-1浓硫酸反应可以得到SO2的分子总数为9NA |
NA 表示阿伏加德罗常数,下列说法中正确的是
| A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B.2 g H2所含有的原子数目是NA |
| C.18 g H2O在标准状况下的体积是22.4 L |
| D.在标准状况时,20 mL NH3与60 mL O2所含的分子个数比为2:1 |
下列叙述中正确的是( )
| A.1 mol H2O的质量是18g/mol | B.硫酸根离子的摩尔质量是96g |
| C.CO2的摩尔质量是44g/mol | D.HCl的相对分子质量是36.5g/mol |
0.5 molNa2SO4中含有Na+的数目是( )个。
| A.3.01×1023 | B.6.02×1023 | C.0.5 | D.1 |