题目内容
下列化学用语正确的是
A.乙烯分子的电子式  |
B.硫原子的结构示意图  |
| C.淀粉的化学式 (C6H10O5)n |
| D.硫酸铁的电离方程式 Fe2(SO4)3 = 2Fe2+ + 3SO42ˉ |
C
解析试题分析:A、C原子之间共用2对电子,故错;B、硫原子的最外层是6个电子,故错;D、铁是+3价,故错。故选C。
考点:电子式的书写 原子的结构示意图的书写 化学式的书写 电离方程式的书写

练习册系列答案
相关题目
还原某二价金属的氧化物4克,需0.2mol电子,则该金属元素的相对原子质量为( )
| A.24 | B.40 | C.56 | D.64 |
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.已知N2(g)+3H2(g)  2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1 2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1 |
| B.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |
| C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| D.2.9g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.01NA个 |
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
| A.16g | B.32g | C.64g /mol | D.32g /mol |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.标准状况下11.2 L NO和11.2 L O2混合后所得气体分子数为NA |
| B.7.1 g Cl2与足量的NaOH溶液反应转移的电子数为0.2NA |
| C.25℃、1.01×105 Pa时,80 g SO3中含有的原子数为4NA |
| D.NA个CO分子和0.5 mol CH4的质量比为7∶4 |
以NA表示阿伏加德罗常数,下列说法中正确的是( )
| A.标准状况下,11.2L水中含有的分子数为0.5NA |
| B.1.8g的NH4+离子中含有的电子数为2NA |
| C.常温、常压下,48g臭氧含有的氧原子数为3NA |
| D.常温、常压下,11.2L氧气所含原子数为NA |
下列生活常见现象中,没有涉及化学变化的是
| A.光合作用 | B.海水晒盐 | C.铁钉生锈 | D.石灰岩风化 |
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是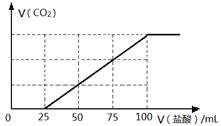
| A.原NaOH溶液的浓度为0.1 mol/L |
| B.通入CO2的体积为448 mL |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) =" 1:" 3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) =" 2:" 1 |
实验室里需用480 mL 0.1 mol/L的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作正确的是( )
| A.称取7.68g硫酸铜,加入500mL水 |
| B.称取12.0g胆矾配成500mL溶液 |
| C.称取8.0g硫酸铜,加入500mL水 |
| D.称取12.5g胆矾配成500mL溶液 |