下列叙述中指定粒子数目一定大于NA的是
| A.11.2L氧气和臭氧的混合气体所含的原子数 |
| B.1mol CaC2固体中含阴离子总数 |
| C.1L1mol/LCH3COOH溶液中所含分子总数 |
| D.1molCl2参加化学反应获得的电子数 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.室温下H2O2分解得到16 g O2,转移的电子数为2NA |
| B.含1mol H2SO4的浓硫酸与足量铜反应转移的电子总数为NA |
| C.标准状况下11.2 L CO和H2的混合气体完全燃烧消耗O2的量为0.25NA |
| D.相同物质的量OH-和CH3+含有相同数目的电子 |
用NA表示阿伏加德罗常数的值,下列说法不正确的是
| A.12.0g熔融的NaHSO4中含有的阳离子数为0.1NA |
| B.常温下,5.6gFe投入到足量浓硝酸中,转移电子数为0.3 NA |
| C.2 mol SO2和1 mol O2在一定条件下充分反应后,所得混合气体的分子数大于2 NA |
| D.足量的锌与一定量的浓硫酸反应生成1 mol气体时,转移的电子数为2NA |
NA表示阿伏伽德罗常数,下列判断正确的是( )
| A.在18 g18O2中含有NA个氧原子 |
| B.标准状况下,22.4L空气含有NA个单质分子 |
| C.1 mol Cl2参加反应转移电子数一定为2 NA |
| D.含NA个Na+ 的Na2O溶解于1L水中,Na+ 的物质的量浓度为1mol·L—1 |
下列化学用语使用不正确的是( )。
A.Na+的结构示意图为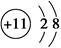 |
| B.明矾的化学式为KAl(SO4)2·12H2O |
| C.聚乙烯的结构简式为CH2===CH2 |
| D.高氯酸(HClO4)中氯元素的化合价为+7 |
下列有关化学实验的描述中正确的是( )
| A.将40 g NaOH溶于1 L蒸馏水中,该溶液的物质的量浓度为1 mol·L-1 |
| B.配制一定物质的量浓度的NaCl溶液,如果NaCl固体中含有Na2CO3,所配制溶液中c(Na+)将偏低 |
| C.将2.5 g CuSO4·5H2O溶解在97.5 g水中,配制质量分数为2.5%的CuSO4溶液 |
| D.把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中c(Cl-)="5" mol·L-1 |
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
| A.2 mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.7.5 mol·L-1 |
设NA代表阿伏加德罗常数的数值。已知C2H4和C3H6的混合物的质量为a g,则该混合物( )
| A.所含共用电子对数目为(+1)NA |
| B.所含碳氢键数目为NA |
C.燃烧时消耗的O2一定是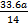 L L |
D.所含原子总数为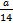 NA NA |
在标准状况下①6.72 L CH4②3.01×1023个HCl分子 ③13.6 g H2S④0.2 mol NH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
| A.abc | B.bcd | C.acd | D.abcd |
 KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA