题目内容
在标准状况下①6.72 L CH4②3.01×1023个HCl分子 ③13.6 g H2S④0.2 mol NH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
| A.abc | B.bcd | C.acd | D.abcd |
D
解析

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.常温常压下,3.36L NO2和水反应转移的电子数为0.1NA |
| B.1 molNa2O2与足量的水反应,转移的电子数为2NA |
| C.在常温常压下,1molFe与1molCl2充分反应,转移的电子数约为3NA |
| D.在1 L lmol·L-1的氨水中,含有的NH3与NH3·H2O分子的总数小于1mol |
还原某二价金属的氧化物4克,需0.2mol电子,则该金属元素的相对原子质量为( )
| A.24 | B.40 | C.56 | D.64 |
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.已知N2(g)+3H2(g)  2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1 2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1 |
| B.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |
| C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| D.2.9g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.01NA个 |
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为 ( )。
| A.2∶7 | B.5∶4 | C.2∶1 | D.7∶2 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )。
| A.1 mol Al3+含有的核外电子数为3NA |
| B.1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| C.室温下,10 L pH=1的硫酸溶液中含有的H+数为2NA |
| D.室温下,10 L pH=13的NaOH溶液中含有的OH-数为NA |
下图是NaCl、MgSO4的溶解度曲线。下列说法正确的是( )。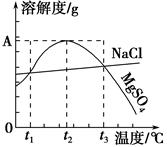
| A.只有在t1℃时,NaCl和MgSO4的溶解度才相等 |
| B.t1℃~t2℃,MgSO4的溶解度随温度升高而减小 |
| C.在t2℃时,MgSO4饱和溶液的溶质质量分数最大 |
| D.把MgSO4饱和溶液的温度从t3℃降至t2℃时,溶液的物质的量浓度减小 |
下列化学用语使用不正确的是( )。
A.Na+的结构示意图为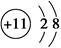 |
| B.明矾的化学式为KAl(SO4)2·12H2O |
| C.聚乙烯的结构简式为CH2===CH2 |
| D.高氯酸(HClO4)中氯元素的化合价为+7 |
 KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA