氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是
| A.H2O2分子中只存在极性键 |
B.NH3的结构式为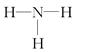 |
C.HCl的电子式为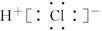 |
D.H2O的比例模型为 |
16O和18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是
| A.16O2与18O2互为同分异构体 |
| B.16O与18O核外电子排布方式不同 |
| C.通过化学变化可以实现16O与18O间的相互转化 |
| D.标准状况下,1.12 L16O2和1.12 L18O2均含0.1NA个氧原子 |
下列有关化学用语,使用正确的是
A.氯原子的原子结构示意图: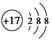 |
B.NH4Cl的电子式: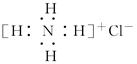 |
C.原子核内有10个中子的氧原子: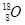 |
| D.聚乙烯的结构简式:CH2=CH2 |
铁氧体(Fe3O4)法是处理含铬废水的常用方法,其原理是用FeSO4把废水中的Cr2O72-还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物(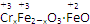 )。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( )
)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( )
| A.x=1,a=5 | B.x=0.5,a=8 |
| C.x=1,a=10 | D.x=0.5,a=10 |
把一块镁铝合金投入到1 mol·L-1盐酸中,待合金完全溶解后,再往溶液里加入1 mol·L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示。下列说法中错误的是( )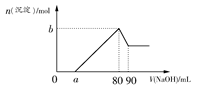
| A.盐酸的体积为80 mL |
| B.a的取值范围为0<a<50 |
| C.n(Mg2+)<0.025 mol |
| D.当a值为30时,b值为0.01 |
把一块镁铝合金投入到1 mol/L盐酸里,待合金完全溶解后,往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图A所示。下列说法中不正确的是( )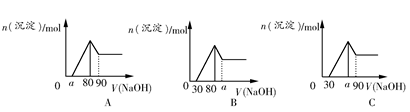
| A.a的取值范围为0≤a<50 |
B.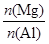 的最大值为2.5 的最大值为2.5 |
| C.若将关系图改为图B,则a的取值范围为80<a<90 |
| D.若将关系图改为图C,则a的取值范围为75<a<90 |
已知Q与R的摩尔质量之比为9:22,在反应X+2Y=2Q+R中,当1.6 g X和Y完全反应后生成4.4 g R,则参与反应的Y和生成物Q的质量之比为( )
| A.46:9 | B.32:9 | C.23:9 | D.16:9 |
下列各项叙述正确的是( )
| A.由同种元素组成的物质肯定属于纯净物 |
| B.具有相同质子数的粒子都属于同种元素 |
| C.一种元素可有多种离子,但只有一种显电中性的原子 |
| D.有新单质生成的化学反应,不一定都属于氧化还原反应 |