题目内容
已知Q与R的摩尔质量之比为9:22,在反应X+2Y=2Q+R中,当1.6 g X和Y完全反应后生成4.4 g R,则参与反应的Y和生成物Q的质量之比为( )
| A.46:9 | B.32:9 | C.23:9 | D.16:9 |
D
解析

练习册系列答案
相关题目
1mol SO2和1mol SO3具有相同的
①分子数 ②原子总数 ③硫原子数 ④氧原子数
| A.①②③ | B.①④ | C.②④ | D.①③ |
若NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.22 g乙醛中含有3 NA个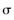 键 键 |
| B.lmol C12与足量Fe完全反应,反应中转移3 N A个电子 |
C.对于Si+O2 SiO2,每当形成2 NA个Si-O键,需断开NA个Si--Si键 SiO2,每当形成2 NA个Si-O键,需断开NA个Si--Si键 |
| D.氯元素的某种核素的质量为ag,该核素的摩尔质量为aNAg/mol |
以NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA |
| B.28gCO中所含的原子数为2NA |
| C.1L 0.1mol/LNa2CO3溶液中,含有CO32— 数为0.1NA |
| D.22.4LH2的分子数为NA |
设阿伏加德罗常数为NA,下列说法正确的是
| A.在1L1mol?L-1的盐酸溶液中含有NA个HCl分子 |
| B.假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA |
| C.标准状况下,11.2 L CCl4中含有的C—Cl 键的个数为2NA |
| D.46gNO2和N2O4混合气体降温到标况,其中含有原子总数为3NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |
某硝酸铵样品中混有另一种氮肥,经测定该样品中含氮38%,则该样品中可能混有的氮肥是( )。
| A.NH4HCO3 | B.(NH4)2SO4 | C.NH4Cl | D.CO(NH2)2 |
铁氧体(Fe3O4)法是处理含铬废水的常用方法,其原理是用FeSO4把废水中的Cr2O72-还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物(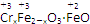 )。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( )
)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( )
| A.x=1,a=5 | B.x=0.5,a=8 |
| C.x=1,a=10 | D.x=0.5,a=10 |
科学家在利用无土栽培培养一些名贵花卉时,培养液中添加了多种必需元素,其配方如下,其中植物根吸收最少的离子是( )。
| 离子 | K+ | Mg2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
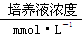 | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
A.Zn2+ B.SO42- C.Ca2+ D.H2PO4-