下列说法中正确的是
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为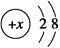 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为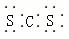 |
| D.中子数为18的氯原子可表示为18Cl |
一定体积的溶质质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质的质量分数恰好增大1倍,溶液体积变为62.5 mL。则浓缩后溶液的物质的量浓度为
| A.2.2 mol·L-1 | B.4 mol·L-1 |
| C.5 mol·L-1 | D.6.25 mol·L-1 |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果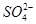 的浓度为0.2 mol·L-1,当加入等体积0.2 mol·L-1KOH溶液时,生成的沉淀恰好完全溶解,(忽略溶液中少量的H+和OH-)则反应后混合溶液中K+的浓度约是
的浓度为0.2 mol·L-1,当加入等体积0.2 mol·L-1KOH溶液时,生成的沉淀恰好完全溶解,(忽略溶液中少量的H+和OH-)则反应后混合溶液中K+的浓度约是
| A.0.125 mol·L-1 | B.0.225 mol·L-1 |
| C.0.250 mol·L-1 | D.0.450 mol·L-1 |
下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是
| A.要配制100 mL 1 mol·L-1 NaOH溶液,需在白纸上称4 g NaOH固体,并且称量速度较慢 |
| B.称量时托盘天平的砝码已被锈蚀 |
| C.溶解或稀释溶质时烧杯尚未干燥 |
| D.定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4L正丁烷和异丁烷的混合物中所含共用电子对数为14NA |
| B.常温常压下,15.0g甲醛与葡萄糖的混合物中含有氢原子的数目为NA |
| C.60g SiO2晶体所含Si—O键的数目为2NA ,78 g苯含有C=C双键的数目为3NA |
D.将CO2通过Na2O2使其增重a g时,反应中转移电子数为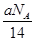 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是(相对原子质量:D-2 O-16 Cu-64)
| A.18 g的D216O中含有的中子数为9 NA |
| B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C.33.6 L NO2溶于足量的水得到的溶液中含有的NO3-数为NA |
| D.32 g铜发生氧化还原反应,一定失去NA个电子 |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,44 g CO2含有nA个C原子 |
| B.1 L 0.1 mol·L-1 Na2S溶液中含有0.1 nA个S2— |
| C.0.1 mol Na与足量O2反应,转移0.2 nA个电子 |
| D.标准状况下,22.4 L 的CCl4含有4 nA个Cl原子 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标况下,11.2L乙烷中含有共价键的数目为3NA |
| B.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2NA |
| C.常温下,22.4L甲烷中含有的电子数为10NA |
| D.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.1mol Cl2与过量的镁铁反应,转移2nA个电子 |
| B.常温下,16g CH4含有8nA个电子 |
| C.1L 0.5 mol·L-1Na2SO4溶液中含有nA个SO42- |
| D.常温常压下,22.4LCO2含有nA个CO2分子 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1molH2O2中含有的电子数为16NA |
| B.标准状况下,11.2L Br2中含Br—Br键数为0.5NA |
| C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子 |
| D.1 L 0.1 mol ·L-1NaHCO3溶液中含有0.1NA 个HCO3 — |