题目内容
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4L正丁烷和异丁烷的混合物中所含共用电子对数为14NA |
| B.常温常压下,15.0g甲醛与葡萄糖的混合物中含有氢原子的数目为NA |
| C.60g SiO2晶体所含Si—O键的数目为2NA ,78 g苯含有C=C双键的数目为3NA |
D.将CO2通过Na2O2使其增重a g时,反应中转移电子数为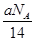 |
B
解析试题分析:A项中,标准状况下,22.4L丁烷是1mol,正丁烷(CH3CH2CH2CH3)和异丁烷[(CH3)CHCH3]分子所含共用电子对数都为13,故A错;B项中,甲醛与葡萄糖的实验式都是CH2O,故15.0g甲醛与葡萄糖的混合物中含有氢原子的数目为NA说法正确;C项中,SiO2晶体平均1个Si有4个Si—O键,所以60g SiO2晶体所含Si—O键的数目为4NA ;苯分子中不含>C=C<双键,故不正确;D项中,将CO2通过Na2O2使其增重a g(增重是CO—28),反应中转移电子数 (1Na2O2转移1e-)为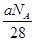 ,故说法错误。
,故说法错误。
考点:用NA为阿伏加德罗常数的值来表示微粒数目。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
下列化学用语或模型正确的是
A.氯化氢的电子式: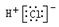 |
| B.8个中子的碳原子:12C |
C.硫离子结构示意图: |
D.CH4分子的比例模型: |
NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.由D和18O所组成的水11g,所含的中子数为4NA |
| B.常温常压下,8gO2含有4 NA个电子 |
| C.25℃时,pH=13的1LBa(OH)2溶液中含有OH—的数目为0.2 NA |
| D.1L1mol/L的NaAlO2水溶液中含有的氧原子数为2NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1molH2O2中含有的电子数为16NA |
| B.标准状况下,11.2L Br2中含Br—Br键数为0.5NA |
| C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子 |
| D.1 L 0.1 mol ·L-1NaHCO3溶液中含有0.1NA 个HCO3 — |
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
| A.3.2 g | B.4.0 g | C.4.2 g | D.4.6 g |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 L 0.1 mol·L-1的氨水中含有NH3·H2O分子数为0.1NA |
| B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| C.标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D.一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
用NA表示阿伏加德罗常数,下列说法中正确的是
A.84 g NaHCO3晶体中含有NA个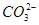 |
| B.9.2 g NO2和N2O4的混合气中含有的氮原子数为0.2NA |
| C.标准状况下,11.2 L臭氧中含NA个氧原子 |
| D.78 g Na2O2与足量的CO2反应,电子转移个数为2NA |
设NA表示阿伏加德罗常数的值。下列叙述正确的是( )。
| A.42 g C3H6中含有的共用电子对数目为8 NA |
| B.电解饱和食盐水时,当0.1 mol NaCl反应时,转移的电子数为0.1 NA |
| C.常温常压下,22.4 L N2和O2的混合气体中含有的分子数目为NA |
| D.1 L 0.01 mol·L-1 KAl(SO4)2溶液中含有的阳离子数目为0.02 NA |