下列表示物质结构的化学用语或模型正确的是
| A.二氧化碳的结构式:O=C=O |
B.HF的电子式: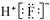 |
C.Cl-离子的结构示意图: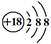 |
D.CH4分子的球棍模型: |
下列物质中,既有离子键,又有共价键的是
| A.CaCl2 | B.Na2O | C.H2O | D.NH4Cl |
自瑞士ETH天文研究所的Ansgar Grimberg等的研究结果表明,太阳气体中存在大量的20Ne和22Ne。下列关于20Ne和22Ne的说法正确的是
| A.20Ne和22Ne互为同位素 | B.20Ne和22Ne是同一种核素 |
| C.20Ne的原子核中有20个质子 | D.22Ne的原子核中有22个中子 |
科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们互称为
| A.同种物质 | B.同分异构体 | C.同素异形体 | D.同位素 |
下列说法正确的是
| A.欲配制1.00L 1.00mol·L-1的NaCI溶液,可将58.5g NaC1溶于1.00L水中 |
| B.0.2mol Na2O2与足量水反应,转移电子数为0.4NA |
| C.同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 |
| D.1.0L 1.0mol ·L-l的Na2CO3水溶液中含有的氧原子数大于2NA |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A.H2O的电子式: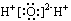 |
B.质量数为14的碳原子: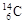 |
C.CO2的比例模型: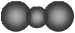 |
D.Cl-的结构示意图: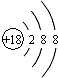 |
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |
下列化学用语正确的是
A.NH4H的电子式: |
| B.硬脂酸的分子式为:C17H35COOH |
C.基态Mg原子的核外电子轨道表示式: |
| D.Cr元素的外围电子排布式:3d54S1 |
向一定量的Fe、FeO、Fe2O3的混合物中,加入200mL2 mol/L的盐酸,恰好完全反应并放出标准状况下224mL气体;向所得溶液中加入KSCN溶液后无血红色出现,则所得溶液中Fe2+的物质的量浓度为(假设反应后溶液体积仍为200mL)
| A.0.5mol·L-1 | B.l mol·L-1 | C.2mol·L-1 | D.0.1mol·L-1 |
NA代表阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,0.1NA个乙炔分子完全燃烧需要的O2的体积约为11.2L |
| B.标准状况下,11.2L乙烯分子中含有的碳碳共用电子对数目为0.5NA |
| C.15g乙烷分子中含有的碳氢键数目为3NA |
| D.常温常压下,1 mol氦气含有的核外电子数为4 NA |