设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,30 g的2-丙醇中含有羟基的数目为0.5 NA |
| B.标准状况下,11.2 L乙炔中含有共用电子对的数目为1.5NA |
| C.1 mol·L-1的碳酸钠溶液中含有CO32-的数目小于NA |
| D.常温下,1 molO2和O3的混合气体中含有氧原子的数目为2.5NA |
下列有关化学用语表示正确的是
A.HClO的电子式: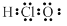 | B.硫离子结构示意图: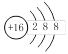 |
| C.丙醛的结构简式:CH3CH2COH | D.碳酸的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.25℃时,pH=13的氨水中含有OH-的数目为0.1NA |
| B.1 mol Na被完全氧化生成Na2O2,转移电子的数目为NA |
| C.标准状况下,2.24 LNO2与水反应生成NO3-的数目为0.1NA |
| D.4.0 g H2与足量N2完全反应生成NH3,反应中断裂共价键的总数为2NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是(相对原子质量:N-14 O-16)
| A.23gNO2和N2O4的混合气体中含有的氮原子数为0.5NA |
| B.标准状况下,2.24 L乙醇中含有的C—H数目为0.5NA |
| C.1 mol·L-1的NaClO溶液中所含ClO-的数目为NA |
| D.室温下H2O2分解得到16 g O2,转移的电子数为2NA |
设NA为阿伏伽德罗常数的值。下列说正确的是
| A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA |
| B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.5NH4NO3△2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA |
NA表示阿伏加德罗常数,下列叙述正确的是
| A.lmol FeI2与足量氯气反应时转移的电子数为2NA |
| B.2 L0.5 mol ? L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C.1 mol Na202固体中含离子总数为4NA |
| D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6 NA |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B.0.1mol丙烯酸中含有双键的数目为0.1NA |
| C.标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
下列关于化学用语的表示正确的是s
A.过氧化钠的电子式: |
B.质子数为35、中子数为45的溴原子: |
C.硫离子的结构示意图: |
D.间二甲苯的结构简式: |
设NA为阿伏伽德罗常数的数值。下列说法正确的是
| A.1mol甲苯含有6NA个C-H键 |
| B.18gH2O含有10NA个质子 |
| C.标准状况下,22.4L氨水含有NA个NH3分子 |
| D.56g铁片投入足量浓硫酸中生成NA个SO2分子 |
设阿伏加德罗常数的值为NA,则下列说法正确的是
| A.标准状况下,11.2L CCl4所含的分子数为0.5NA |
| B.常温常压下,4.2g C2H4和C8H16的混合物中含有的碳原子数为0.3NA |
| C.7.8g苯分子中碳碳双键的数目为0.3 NA |
| D.6.4gCu与20mL10 mol·L-1浓硫酸反应,转移的电子数为0.2NA |