0 95787 95795 95801 95805 95811 95813 95817 95823 95825 95831 95837 95841 95843 95847 95853 95855 95861 95865 95867 95871 95873 95877 95879 95881 95882 95883 95885 95886 95887 95889 95891 95895 95897 95901 95903 95907 95913 95915 95921 95925 95927 95931 95937 95943 95945 95951 95955 95957 95963 95967 95973 95981 203614



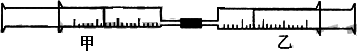
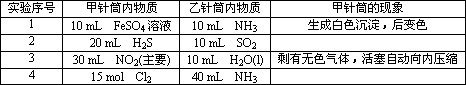

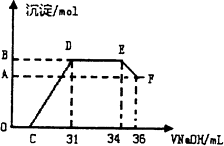


 .
.