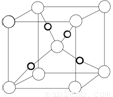
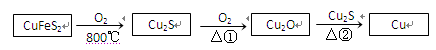(14分)
(1)反应Fe(s)+CO2(g) FeO(s)+CO(g)
△H1,平衡常数为K1
FeO(s)+CO(g)
△H1,平衡常数为K1
反应Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常数为K2
FeO(s)+H2(g) △H2,平衡常数为K2
在不同温度时K1、K2的值如下表:
|
|
700℃ |
900℃ |
|
K1 |
1.47 |
2.15 |
|
K2 |
2.38 |
1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) △H
,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应
CO(g) + H2O(g) △H
,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应
CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
②能判断CO2(g) + H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示:
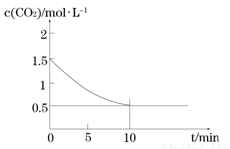
① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为 mol·L-1。
②下列措施中能使平衡时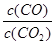 增大的是 (填序号)
增大的是 (填序号)
A.升高温度
B.增大压强
C.充入一定量的CO2
D.再加入一定量铁粉
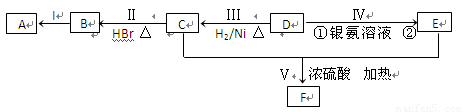
(15分)某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,

并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性。
(1)写出甲中反应的离子方程式 。
(2)为完成上述实验,正确的连接顺序为A连 ,B连 (填接口字母)。
(3)乙装置中X试剂可以是 ,丙装置中Y试剂的作用是 。
(4)测定Cu的相对原子质量。将w g CuO置于硬质玻璃管中,足量的H2与之充分反应后,按以下两个方案测得的数据计算Cu的相对原子质量。
|
方 案 质 量 |
方案一 |
方案二 |
|
U型管+固体 |
硬质玻璃管+固体 |
|
|
反应前质量/g |
a |
c |
|
完全反应后质量/g |
b |
d |
你认为方案 较佳,另一个方案得到的Cu的相对原子质量会 (填“偏低”、“偏高”)。按较佳方案计算,得到Cu的相对原子质量是 。