根据下列实验现象,所得结论正确的是( )
A.A
B.B
C.C
D.D
| 实验 | 实验现象 | 结论 |
| A | 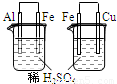 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Cu>Fe |
| B | 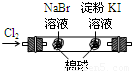 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 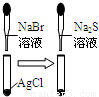 白色固体先变为淡黄色,后变为黑色 | 溶解性AgCl>AgBr>Ag2S |
| D | 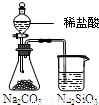 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A.A
B.B
C.C
D.D
Ⅰ.氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
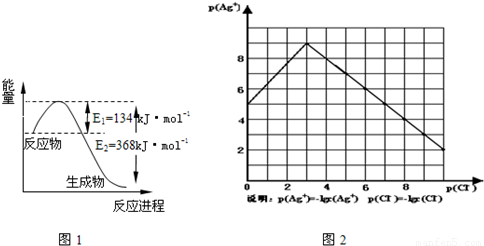
(1)图1是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和 CO反应的热化学方程式
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:请完成下列问题;
①试比较K1、K2的大小,K1 K2(填写“>”、“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是 (填序号字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.υ(N2)(正)=3υ(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数的值为 .当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的
υ(N2)(正) υ(N2)(逆) (填写“>”、“=”或“<”=)
Ⅱ.沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合
物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-═[AgCl2]-,图2是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
(1)由图知该温度下AgCl的溶度积常数为 .
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
(3)设计实验证明S(AgCl)>S(AgI)>S(Ag2S),实验方案是 .
(4)若在AgCl形成的浊液中滴加氨水有什么现象? .发生反应的离子方程式为 .

(1)图1是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和 CO反应的热化学方程式
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1 K2(填写“>”、“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是 (填序号字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.υ(N2)(正)=3υ(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数的值为 .当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的
υ(N2)(正) υ(N2)(逆) (填写“>”、“=”或“<”=)
Ⅱ.沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合
物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-═[AgCl2]-,图2是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
(1)由图知该温度下AgCl的溶度积常数为 .
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
(3)设计实验证明S(AgCl)>S(AgI)>S(Ag2S),实验方案是 .
(4)若在AgCl形成的浊液中滴加氨水有什么现象? .发生反应的离子方程式为 .
氯化铜晶体中常含FeC12杂质,为制得纯净氯化铜晶体,首先将其溶于稀盐酸中,然后按下面所示操作步骤进行提纯.
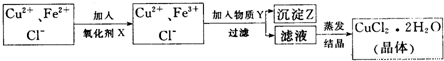
已知:(1)下列物质中,最适合作为氧化剂X的是 (填序号)
A.H2O2B.KMnO4C.NaC1O D.浓硫酸
写出加入X后发生反应离子的方程式 .
(2)加入的物质Y可以是 ,目的是
(3)某同学利用反应Cu+2H+ Cu2++H2↑设计实验来
制取氯化铜溶液.该同学设计的装置应该为 (填“原电池”或“电解池”).请画出该同学设计的装置图,并指明电极材料和电解质溶液.
(4)从CuC12稀溶液中得到CuC12?2H2O晶体,在蒸发结晶的过程中,为了防止Cu2+的水解,应采取的措施是 .
0 67792 67800 67806 67810 67816 67818 67822 67828 67830 67836 67842 67846 67848 67852 67858 67860 67866 67870 67872 67876 67878 67882 67884 67886 67887 67888 67890 67891 67892 67894 67896 67900 67902 67906 67908 67912 67918 67920 67926 67930 67932 67936 67942 67948 67950 67956 67960 67962 67968 67972 67978 67986 203614

| 氢氧化物开始沉淀时的pH | 氯氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
A.H2O2B.KMnO4C.NaC1O D.浓硫酸
写出加入X后发生反应离子的方程式 .
(2)加入的物质Y可以是 ,目的是
(3)某同学利用反应Cu+2H+ Cu2++H2↑设计实验来
制取氯化铜溶液.该同学设计的装置应该为 (填“原电池”或“电解池”).请画出该同学设计的装置图,并指明电极材料和电解质溶液.
(4)从CuC12稀溶液中得到CuC12?2H2O晶体,在蒸发结晶的过程中,为了防止Cu2+的水解,应采取的措施是 .
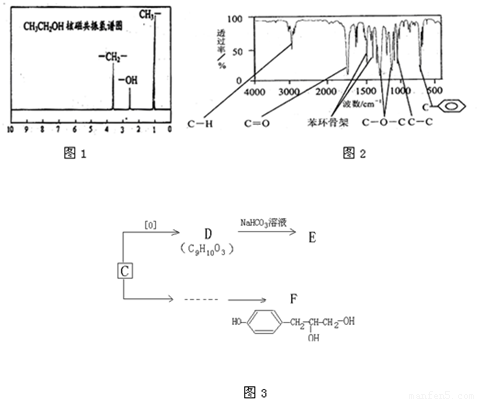
 B
B C…→H合成反应流程图. .
C…→H合成反应流程图. .