利用焦炭或天然气制取廉价的CO和H2,再用于有机合成是目前工业生产的重要途径.回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
已知1mol H2O (g)转变为1mol H2O(l)时放出44.0kJ热量.则CH4和水蒸气在高温下反应生成1mol H2的反应热为______.
(2)用CO和H2在一定条件下合成甲醇:CO+2H2?CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是______.
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:
CH2=CH2 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH
某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O  CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?______.
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热 |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
(2)用CO和H2在一定条件下合成甲醇:CO+2H2?CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是______.
| 反应温度/℃ | 平衡常数 | 反应温度/℃ | 平衡常数 |
| 667.30 | 200 | 1.909×10-2 | |
| 100 | 12.92 | 300 | 2.42×10-4 |
CH2=CH2
 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
 CO+H2 CH4+H2O
CO+H2 CH4+H2O  CO+3H2
CO+3H2假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?______.
(1)下列有关实验的基本操作及安全知识的叙述,正确的是______(填序号).
A.附着于试管内壁的苯酚,可用碱液洗涤 B.用结晶法可以除去硝酸钾中混有的少量氯化钠
C.切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割
D.实验时,不慎打翻燃着的酒精灯,可立即用湿抹布盖灭火焰
E.浓硫酸不小心沾到皮肤上,立刻用稀烧碱溶液洗涤
F.在氢氧化铁胶体中滴加少量稀硫酸会产生沉淀
(2)下表是某种常见金属的部分性质:
将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体.试回答:
①推断该金属可能的一种用途______,该金属的活动性比铜______(填“强”或“弱”).
②请自选试剂,设计不同的实验探究该金属与铁的活动性强弱,并完成下表:
A.附着于试管内壁的苯酚,可用碱液洗涤 B.用结晶法可以除去硝酸钾中混有的少量氯化钠
C.切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割
D.实验时,不慎打翻燃着的酒精灯,可立即用湿抹布盖灭火焰
E.浓硫酸不小心沾到皮肤上,立刻用稀烧碱溶液洗涤
F.在氢氧化铁胶体中滴加少量稀硫酸会产生沉淀
(2)下表是某种常见金属的部分性质:

将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体.试回答:
①推断该金属可能的一种用途______,该金属的活动性比铜______(填“强”或“弱”).
②请自选试剂,设计不同的实验探究该金属与铁的活动性强弱,并完成下表:
| 猜想 | 验证方法 | 预测实验现象 |
| ______ | ______ | ______ |
| ______ | ______ | ______ |
根据侯德榜制碱法原理并参考下表的数据,实验室制备纯碱Na2CO3的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30~35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得Na2CO3固体.四种盐在不同温度下的溶解度(g/100g水)表①>35℃NH4HCO3会有分解
请回答:
(1)反应温度控制在30~35℃,是因为若高于35℃,则______,若低于30℃,则______;为控制此温度范围,采取的加热方法为______;
(2)加料完毕后,继续保温30分钟,目的是______.静置后只析出NaHCO3晶体的原因是______.用蒸馏水洗涤NaHCO3晶体的目的是除去______杂质(以化学式表示);
(3)过滤所得的母液中含有______(以化学式表示),需加入______,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl;
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点),所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V2 mL.写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)=______.
0 67734 67742 67748 67752 67758 67760 67764 67770 67772 67778 67784 67788 67790 67794 67800 67802 67808 67812 67814 67818 67820 67824 67826 67828 67829 67830 67832 67833 67834 67836 67838 67842 67844 67848 67850 67854 67860 67862 67868 67872 67874 67878 67884 67890 67892 67898 67902 67904 67910 67914 67920 67928 203614
| 温度溶解度盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
(1)反应温度控制在30~35℃,是因为若高于35℃,则______,若低于30℃,则______;为控制此温度范围,采取的加热方法为______;
(2)加料完毕后,继续保温30分钟,目的是______.静置后只析出NaHCO3晶体的原因是______.用蒸馏水洗涤NaHCO3晶体的目的是除去______杂质(以化学式表示);
(3)过滤所得的母液中含有______(以化学式表示),需加入______,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl;
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点),所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V2 mL.写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)=______.





 合成OHC(CH2)4CHO(用反应流程图表示,注明反应物、反应条件)
合成OHC(CH2)4CHO(用反应流程图表示,注明反应物、反应条件) CH2=CH2
CH2=CH2



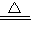 Fe2O3+SO2↑+SO3↑.
Fe2O3+SO2↑+SO3↑.
 N2↑+4H2O↑+Cl2↑+2O2↑
N2↑+4H2O↑+Cl2↑+2O2↑