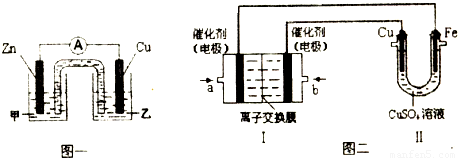
I.图1为向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.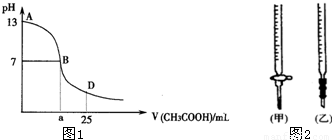
请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?______区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项______.(选填字母)
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是______.
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)大于、小于或等于c(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+).(填“>”、“<”或“=”)
Ⅱ.t℃时,某稀硫酸溶液中c(H+)=10-a mol?L-1,c(OH-)=10-b mol?L-1,已知a+b=13:
(5)该温度下水的离子积常数Kw的数值为______.
(6)该温度下(t℃),将100mL 0.1mol?L-1的稀H2SO4溶液与100mL 0.4mol?L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=______.

请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?______区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项______.(选填字母)
| 锥形瓶中溶液 | 滴定管 中溶液 | 选用 指示剂 | 选用 滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)大于、小于或等于c(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+).(填“>”、“<”或“=”)
Ⅱ.t℃时,某稀硫酸溶液中c(H+)=10-a mol?L-1,c(OH-)=10-b mol?L-1,已知a+b=13:
(5)该温度下水的离子积常数Kw的数值为______.
(6)该温度下(t℃),将100mL 0.1mol?L-1的稀H2SO4溶液与100mL 0.4mol?L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=______.
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同) .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
①由表中数据判断该反应的△H 0(填“>”、“=”或“<”);
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 ,此时的温度为 .
(3)要提高CO的转化率,可以采取的措施是 .
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是 .
A.2c1>c3B.a+b<90.8C.2p2<p3D.α1+α3<1.
0 63173 63181 63187 63191 63197 63199 63203 63209 63211 63217 63223 63227 63229 63233 63239 63241 63247 63251 63253 63257 63259 63263 63265 63267 63268 63269 63271 63272 63273 63275 63277 63281 63283 63287 63289 63293 63299 63301 63307 63311 63313 63317 63323 63329 63331 63337 63341 63343 63349 63353 63359 63367 203614
(1)判断反应达到平衡状态的依据是(填字母序号,下同) .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 ,此时的温度为 .
(3)要提高CO的转化率,可以采取的措施是 .
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡时数据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | akJ | bkJ | ckJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3B.a+b<90.8C.2p2<p3D.α1+α3<1.