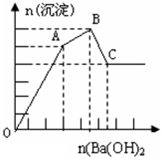
 向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如图所示.
向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如图所示.
沉淀的生成与溶解的pH列于下表.以下推断正确的是
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | ||
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
- A.C点的沉淀为:Fe(OH)3
- B.OA段可能发生的反应有:3Ba2++6OH-+3SO42-+2Fe3+→3BaSO4↓+2Fe(OH)3↓
- C.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-→2BaSO4↓+Al(OH)3↓
- D.据图计算原溶液中c(Cl-)>c(SO42-)
将一质量分数为ω的KOH溶液蒸发掉m g水后,质量分数恰好变为3ω,体积为VL(溶液中无晶体析出),则浓缩后溶液的物质的量浓度为
- A.
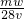 mol?L-1
mol?L-1 - B.
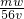 mol?L-1
mol?L-1 - C.
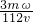 mol?L-1
mol?L-1 - D.
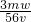 mol?L-1
mol?L-1