已知① CH3CH2OH CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2 BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
|
|
乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
通常状况下的状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/g·cm-3 |
0.79 |
2.2 |
0.71 |
|
熔点/℃ |
-130 |
9 |
-116 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。

(1)仪器E的名称是 。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作 用是 (填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是 。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是 。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于 (填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是 。说明制备1,2-二溴乙烷的反应已经结束的实验现象是 。

 分子中含有1个手性碳原子
分子中含有1个手性碳原子  C6H50H+2C032-
C6H50H+2C032- CH3CH20H
CH3CH20H 2CuO↓+C5H12COONa+3H2O
2CuO↓+C5H12COONa+3H2O 脱去2分子水:
脱去2分子水: 
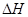 =
+28.7 kJ·mol-1
=
+28.7 kJ·mol-1 表示物质的摩尔质量,则下列各式中正确的是
表示物质的摩尔质量,则下列各式中正确的是 (丁)=
(丁)= O2(g)=CO(g)
O2(g)=CO(g)  =-111.0 KJ·mol-1
=-111.0 KJ·mol-1