己知反应A(g) +
B(g)  C(g)
+ D(g)的平衡常数K值与温度的关系如表所示。830℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
C(g)
+ D(g)的平衡常数K值与温度的关系如表所示。830℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
|
温度/℃ |
700 |
830 |
1200 |
|
K值 |
1.7 |
1.0 |
0.4 |
A.达到平衡后,B的转化率为50%
B.增大压强,正、逆反应速率均加快
C.该反应为吸热反应,升高温度,平衡正向移动
D.反应初始至平衡,A的平均反应速率v(A) = 0.005 mol·L-1·s-1
钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)Al(NO3)3是制备钠硫电池部件的原料之一。由于Al(NO3)3容易吸收环境中的水分,需要对其进行定量分析。具体步骤如下图所示:

①加入试剂a后发生反应的离子方程式为 。
②操作b为 ,操作c为 。
③Al(NO3)3待测液中,c (Al3+) = mol·L-1(用m、v表示)。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:

①根据下表数据,请你判断该电池工作的适宜温度应控制在 范围内(填字母序号)。
|
物质 |
Na |
S |
Al2O3 |
|
熔点/℃ |
97.8 |
115 |
2050 |
|
沸点/℃ |
892 |
444.6 |
2980 |
a.100℃以下 b.100℃~300℃ c. 300℃~350℃ d. 350℃~2050℃
②放电时,电极A为 极。
③放电时,内电路中Na+的移动方向为 (填“从A到B”或“从B到A”)。
④充电时,总反应为Na2Sx = 2Na + xS(3<x<5),则阳极的电极反应式为 。
某实验小组同学探究铜与硝酸的反应。
(1)用浓硝酸和水按照不同体积比配成不同浓度的硝酸溶液,各取10 mL硝酸溶液分别与铜片反应,实验记录如下:
|
序号 |
浓硝酸与水的体积比 |
实验现象 |
|
Ⅰ |
1:1 |
反应速率快,溶液很快变成蓝色,铜丝表面有大量气泡冒出,气体呈红棕色 |
|
Ⅱ |
1:3 |
反应速率较快,溶液变成蓝色,铜丝表面有大量气泡冒出,气体无色 |
|
Ⅲ |
1:5 |
反应速率慢,微热后速率加快,溶液变成蓝色,铜丝表面有气泡冒出,气体无色 |
铜与稀硝酸反应的离子方程式为 ;若生成标准状况下0.56 L NO气体,反应中被还原的HNO3的质量为 g(小数点后保留两位有效数字)。
依据上表,制备NO气体最适宜的是实验II,理由是 。
(2)为防止有毒气体逸散造成空气污染,该小组同学改进实验装置,如右图所示(夹持仪器略去)。

用该装置进行铜与稀硝酸的反应并验证产生NO气体的性质,实验步骤如下:
Ⅰ.安装好装置后,检查装置气密性。
Ⅱ.打开旋塞C,从B管上端加入所选浓度的硝酸,至铜丝下沿(不接触铜丝)。
Ⅲ.向上移动B管,使A管液面上升至与橡皮塞恰好接触,关闭旋塞C,反应开始。
Ⅳ.当液面重新下降至与铜丝脱离接触时,反应停止。
Ⅴ.打开旋塞C,向下移动B管,使A中迅速进入少量空气,关闭旋塞C,观察现象。
……
①步骤Ⅰ中检查装置气密性的操作是:关闭旋塞C,从B管上端加入水,若观察到 ,说明装置的气密性良好。
②步骤Ⅲ操作的目的是 。
③为使A管内的NO气体完全被溶液吸收,可进一步采取的操作是 ,能确定NO完全被溶液吸收的现象是 。

 (R,R’为烃基或氢)
(R,R’为烃基或氢) (R,R’为烃基)
(R,R’为烃基) 、
、 、 和 。
、 和 。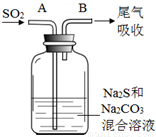
 2H2SO4
2H2SO4 +2H2O
+2H2O H2CO3+2OH¯
H2CO3+2OH¯ +H2O
+H2O