某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.所用HNO3浓度为1.00mol?L-1、2.00mol?L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3的用量为25.0mL、大理石用量为10.00g.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
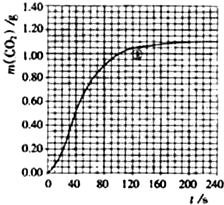
(2)实验①中CO2质量随时间变化的关系见下图:依据反应方程式
CaCO3+HNO3=
Ca(NO3)2+
CO2↑+
H2O,计算实验①在70-90s范围内HNO3的平均反应速率为(忽略溶液体积变化,) (图中70-90s间CO2的质量增加了0.1g)
(3)预期实验结果是(比较三组实验速率的快慢,用代号) 、 、 .
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol?L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 (Ⅲ)实验①和 |
| ② | ||||
| ③ | ||||
| ④ |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(3)预期实验结果是(比较三组实验速率的快慢,用代号)

为了探究硫酸铜对硫酸与锌反应速率的影响,有同学设计了在一定条件下进行如下实验,测量在不同试剂用量的反应条件下获得相同量气体所用的时间.
(1)请完成下表(填写表格中的空白处)(假设溶液混合时体积变化忽略不计)
(2)实验③一段时间后可看到的锌粒表面呈 色.
(3)实验表明②号实验最快,③号实验最慢,可能的原因是
(1)请完成下表(填写表格中的空白处)(假设溶液混合时体积变化忽略不计)
| 试验编号 | ① | ② | ③ |
| 所加0.4moL/LH2SO4 溶液的体积 | 30mL | ||
| 所加0.2 moL/LCuSO4溶液的体积 | 0 | 0.5mL | 5mL |
| 所加蒸馏水的体积 | 5mL | ||
| 探究硫酸铜对硫酸与锌反应速率的影响 | . | ||
| 设计实验室应注意的问题 | |||
(3)实验表明②号实验最快,③号实验最慢,可能的原因是
现甲、乙两化学小组安装两套如图1相同装 置,用以探究影响H2O2分解速率的因素.

(1)仪器a的名称 ;
检查装置气密性的操作为 .
(2)MnO2催化下H2O2分解的化学方程式是 .
(3)甲小组有如下实验设计方案,请帮助完成(所有空均需填满).
(4)甲、乙两小组得出如图2数据.
①由甲组实验π得出的数据可知:浓度越大,H2O2分解速率 ;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,Na202和K2O2溶于水放出气体速率较快的是 ;乙组提出可以用Ba02固体与H2SO4溶液反应制H202,其化学反应方程式为 ;支持这一方案的理由是 .

(1)仪器a的名称
检查装置气密性的操作为
(2)MnO2催化下H2O2分解的化学方程式是
(3)甲小组有如下实验设计方案,请帮助完成(所有空均需填满).
| 实验序号 | 实验目的 | T/K | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 做实验参照 | 298 | 3滴FeCl3溶液 | 10mL2%H2O2 |
| 甲组实验Ⅱ | 298 | 10mL5%H2O2 |
①由甲组实验π得出的数据可知:浓度越大,H2O2分解速率
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,Na202和K2O2溶于水放出气体速率较快的是
(1)已知Na2S2O3+H2SO4═NaSO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择实验 (填实验编号);
若同时选择实验①、实验②、实验③,测定混合液变浑浊的时问,可探究 对化学反应速率的影响.
(2)某同学设计如图实验流程探究Na2S2O3的化学性质.
用离子议程式表示Na2S2O3溶液具有碱性的原因 ,实验操作①中测试时pH试纸的颜色应该接近 .
A.红色 B.深蓝色 C.黄色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的 性.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol?L-1 | c(H2SO4)/mol?L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
若同时选择实验①、实验②、实验③,测定混合液变浑浊的时问,可探究
(2)某同学设计如图实验流程探究Na2S2O3的化学性质.
用离子议程式表示Na2S2O3溶液具有碱性的原因
A.红色 B.深蓝色 C.黄色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大 ,原因是 .
(2)哪一时间段的反应速率最小 ,原因是 .
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变) .
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水、B.NaCl溶液、C.NaNO3溶液、D.CuSO4溶液、E.Na2CO3溶液,你认为可行的是 .
(5)把锌与盐酸的反应设计成原电池,请画出装置示意图,标明正负极,电子流动方向,写出正极的电极反应式 .
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一时间段的反应速率最小
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水、B.NaCl溶液、C.NaNO3溶液、D.CuSO4溶液、E.Na2CO3溶液,你认为可行的是
(5)把锌与盐酸的反应设计成原电池,请画出装置示意图,标明正负极,电子流动方向,写出正极的电极反应式
H2O2是实验室常用的一种化学试剂.
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)实验①和②的目的是 ,实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 .
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是 .

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是 .
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因 ,计算H2O2的初始物质的量浓度 .(保留两位有效数字)
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因
某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响.在常温下按照如下方案完成实验.实验②的反应物应( )
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 无 | |
| ③ | 10mL 5% H2O2溶液 | MnO2 固体 |
| A、5mL 2% H2O2溶液 |
| B、10mL 5% H2O2溶液 |
| C、10mL 2% H2O2溶液 |
| D、5mL 10% H2O2溶液 |
下列有关催化剂的说法中错误的是( )
| A、催化剂就是二氧化锰 | B、催化剂能改变其他物质的化学反应速度 | C、在化学反应前后催化剂的质量没有改变 | D、在化学反应前后催化剂的化学性质没有改变 |

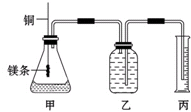 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下: