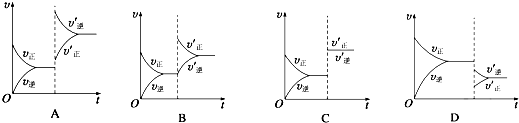
某恒温密闭容器中,可逆反应A(s)?B+C(g)-Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A、产物B的状态只能为固态或液态 | B、平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | C、保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 | D、若开始时向容器中加入1mol B和1mol C,达到平衡时放出热量Q |
如图所示与对应的叙述相符的是( )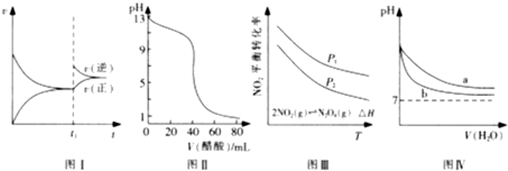

| A、图I可表示N2+3H2?2NH3的速率时间图象,t1时刻改变的条件是升高温度 | B、图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线 | C、图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2 | D、图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水 |
下列说法错误的是( )
| A、当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应 | B、发生有效碰撞的分子一定是活化分子 | C、活化分子间的碰撞一定是有效碰撞 | D、活化分子间每次碰撞不一定发生化学反应 |
下列影响化学反应的本质原因分析错误的是( )
| A、增大反应物浓度,单位体积内活化分子数增多,有效碰撞几率增加 | B、有气体参加的化学反应,若缩小反应容器的体积,主要增大了活化分子的百分数 | C、升高温度,主要增加了反应物分子中活化分子数 | D、加入催化剂后,活化分子数增大,活化分子百分数也增大 |
下列对“活化分子”的说法中不正确的是( )
| A、活化分子之间的碰撞不一定都是有效碰撞 | B、升高温度,可使单位体积内活化分子增多,反应速率加快 | C、对于有气体参加的反应增大压强,可使单位体积内活化分子百分数增加,反应速率加快 | D、催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
在其他条件具备时,若一反应较难进行,则其主要原因可能是( )
①参加反应的分子的能量普遍较低
②参加反应的分子的能量普遍较高
③单位时间内反应物活化分子有效碰撞次数较少
④单位时间内反应物活化分子有效碰撞次数较多
⑤反应物分子中活化分子百分数较小
⑥反应物分子中活化分子百分数较大.
①参加反应的分子的能量普遍较低
②参加反应的分子的能量普遍较高
③单位时间内反应物活化分子有效碰撞次数较少
④单位时间内反应物活化分子有效碰撞次数较多
⑤反应物分子中活化分子百分数较小
⑥反应物分子中活化分子百分数较大.
| A、①③⑤ | B、②④⑥ | C、①④⑥ | D、②③⑤ |
下列有关卤族元素的说法中,正确的是( )
| A、原子半径:F>C1>Br>I | B、最外层电子数:F>C1>Br>I | C、熔、沸点:F2>Cl2>Br2>I2 | D、热稳定性:HF>HCl>HBr>HI |
若用X代表F、Cl、Br、I四种卤族元素,下列属于它们共性反应的是( )
| A、X2+H2=2HX | B、X2+H2O=HX+HXO | C、2Fe+3X2=2FeX3 | D、X2+2NaOH=NaX+NaXO+H2O |
粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )
| A、H2O | B、Zn | C、KI | D、KCl |