题目内容
如图所示与对应的叙述相符的是( )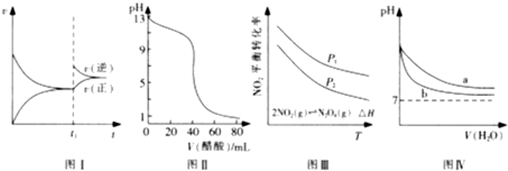

| A、图I可表示N2+3H2?2NH3的速率时间图象,t1时刻改变的条件是升高温度 | B、图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线 | C、图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2 | D、图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水 |
分析:A.升高温度,正逆反应速率都增大;
B.当醋酸的体积是80mL时,混合溶液中存在的溶质是醋酸和醋酸钠,根据醋酸的浓度判断溶液的pH;
C.当温度一定时,增大压强平衡向气体体积减小的方向移动,当压强一定时,升高温度,平衡向吸热反应方向移动,根据温度、压强和二氧化氮的转化率的关系分析;
D.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释两种溶液时,促进一水合氨电离,利用两溶液在稀释时强碱的变化程度大来分析解答.
B.当醋酸的体积是80mL时,混合溶液中存在的溶质是醋酸和醋酸钠,根据醋酸的浓度判断溶液的pH;
C.当温度一定时,增大压强平衡向气体体积减小的方向移动,当压强一定时,升高温度,平衡向吸热反应方向移动,根据温度、压强和二氧化氮的转化率的关系分析;
D.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释两种溶液时,促进一水合氨电离,利用两溶液在稀释时强碱的变化程度大来分析解答.
解答:解:A.对于任何反应来说,升高温度时,正逆反应速率都增大,故A错误;
B.当醋酸的体积是80mL时,混合溶液中存在的溶质是醋酸和醋酸钠,醋酸的物质的量浓度小于0.1mol/L,则溶液的pH大于1,故B错误;
C.当温度一定时,增大压强平衡向正反应方向移动,二氧化氮的转化率增大,则P1>P2,
当压强一定时,升高温度,二氧化氮的转化率减小,则平衡向逆反应方向移动,则正反应是放热反应,△H<0,故C错误;
D.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释溶液促进弱电解质电离,导致稀释溶液氢氧化钠溶液中氢氧根离子浓度变化较大,氨水中氢氧根离子浓度变化较小,pH变化较小,则b是氨水溶液,故D正确;
故选D.
B.当醋酸的体积是80mL时,混合溶液中存在的溶质是醋酸和醋酸钠,醋酸的物质的量浓度小于0.1mol/L,则溶液的pH大于1,故B错误;
C.当温度一定时,增大压强平衡向正反应方向移动,二氧化氮的转化率增大,则P1>P2,
当压强一定时,升高温度,二氧化氮的转化率减小,则平衡向逆反应方向移动,则正反应是放热反应,△H<0,故C错误;
D.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释溶液促进弱电解质电离,导致稀释溶液氢氧化钠溶液中氢氧根离子浓度变化较大,氨水中氢氧根离子浓度变化较小,pH变化较小,则b是氨水溶液,故D正确;
故选D.
点评:本题考查图象题,根据外界条件对反应速率、化学平衡的影响来分析解答,注意分析曲线的变化趋势,难度中等.

练习册系列答案
相关题目