0.1mol/L K2CO3溶液中,若使c(CO32-)更接近0.1mol/L,可采取的措施是( )
| A、加入少量盐酸 | B、加水 | C、加KOH固体 | D、加热 |
关于FeCl3溶液水解的说法错误的是( )
| A、水解达到平衡时加水稀释,平衡向正反应方向移动 | B、浓度为5mol?L-1和0.5mol?L-1的两种FeCl3溶液,其他条件相同时,Fe3+水解程度前者比后者小 | C、有50℃和20℃的同浓度的FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | D、为抑制Fe3+水解,较好地保存FeCl3溶液应加入少量HCl |
向三份0.1mol/L CH3COONa溶液中分别加入少量NH4NO3、Na2CO3、CH3COONa固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
| A、减小、增大、减小 | B、增大、减小、减小 | C、减小、增大、增大 | D、增大、减小、增大 |
为了使Na2S溶液中c(Na+)/c(S2-)的比值变小,可加入的物质是( )
| A、适量KOH溶液 | B、适量H2S气体 | C、适量盐酸 | D、适量NaOH溶液 |
在一定的温度下,下列叙述与图象对应正确的是( )
A、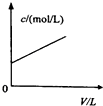 如图中曲线可表示向0.1mol/L CH3COONa溶液中加水稀释的过程中OH-浓度随溶液体积的变化趋势 | B、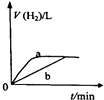 如图中曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)跟同浓度等体积盐酸反应过程中产生H2体积的变化趋势 | C、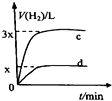 如图中曲线c、d分别表示等质量的铝分别跟过量烧碱溶液、过量盐酸反应过程中产生H2体积的变化趋势 | D、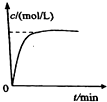 如图中曲线可表示足量锌与一定量稀醋酸反应过程中,Zn2+浓度的变化趋势(假设反应过程中溶液体积保持不变) |
 某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如图所示.据图判断下列叙述中,正确的是( )
某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如图所示.据图判断下列叙述中,正确的是( )| A、Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线 | B、b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同 | C、a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同 | D、c点溶液的导电能力一定比b点溶液导电能力强 |
已知:某酸式盐NaHB在水溶液中,HB-的电离程度小于HB-的水解程度,则下列说法正确的是( )
| A、HB-水解方程式:HB-+H2O?H3O++B2- | B、溶液中离子浓度大小为:c(Na+)=c(HB-)>c(OH-)=c(H+) | C、NaHB的存在抑制了水的电离 | D、相同物质的量浓度溶液的pH:Na2B>NaHB |
常温下,浓度均为0.2mol/L的①(NH4)2SO4溶液②NH4Cl溶液③氨水,其中c(NH4+)大小关系正确的是( )
| A、①>②>③ | B、③>②>① | C、①=②>③ | D、①>②=③ |
向三份0.1mol?L-1的NH4Cl溶液中分别加入少量的Mg、NaOH、SO3固体(忽略溶液体积变化),则NH
浓度的变化依次为( )
+ 4 |
| A、减小、增大、减小 |
| B、增大、减小、减小 |
| C、减小、增大、增大 |
| D、减小、减小、增大 |
下列说法不正确的是( )
| A、水解反应NH4++H2O?NH3?H2O+H+达到平衡后,升高温度平衡正向移动 | B、在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,该现象不足以说明Ksp(BaSO4)与Ksp(BaCO3)大小关系 | C、明矾水解生成Al(OH)3胶体,可用作净水剂 | D、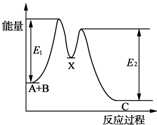 如图所示的反应过程中A+B→X的△H<0,X→C的△H>0 |