常温下,某溶液的pH=5,则由水电离出的c(H+)可能是( )
| A、1×10-6mol/L | B、1×10-7 mol/L | C、1×108 mol/L | D、1×10-9 mol/L |
对于常温下PH为2的盐酸,叙述正确的是( )
| A、c(H+)=c(Cl-)+c(OH-) | B、由H2O电离出的c(H+)=1.0×10-12mol?L-1 | C、与等体积PH=12的氨水混合后所得溶液显酸性 | D、与等体积0.01mol?L-1乙酸钠溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
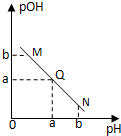 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )| A、N点所示溶液中c(H+)<c(OH-) | B、M点所示溶液导电能力强于Q点 | C、M点水的电离程度大于N点 | D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
在室温下,把80mL盐酸加入120mLNaOH溶液中,所得溶液的pH为12.如果混合前NaOH溶液和盐酸的物质的量浓度相同,它们的浓度是( )
| A、0.05mol/L | B、0.1mol/L | C、0.5mol/L | D、1mol/L |
常温下柠檬水溶液的pH=3,其中c(OH-)是( )
| A、1×10-11mol?L-1 | B、1×10-3mol?L-1 | C、1×10-7mol?L-1 | D、O.1mol?L-1 |
下列溶液:①CH3COOH ②H2SO4 ③HCl ④Ba(OH)2 ⑤NaOH⑥CH3COONa ⑦KCl ⑧NH4Cl其物质的量浓度均为0.1mol/L,pH由小到大排列顺序为( )
| A、②③①⑧⑦⑥⑤④ | B、④⑤⑥⑦⑧①③② | C、③②①⑥⑦⑧④⑤ | D、②③①⑤④⑧⑦⑥ |
下列叙述中一定正确的是( )
| A、任何浓度溶液的酸碱性都可用pH试纸测定 | B、某温度下,pH=6.2的纯水显酸性 | C、25℃时,pH=1的醋酸溶液中c(H+)是pH=2的盐酸溶液中c(H+)的10倍 | D、25℃时,pH=12的NaOH溶液中的n(OH-)=10-2mol |
有人曾建议用AG表示溶液的酸度,AG的定义为AG=lg
.下列表述正确的是( )
| H+ |
| OH- |
| A、在25℃时,若溶液呈中性,则pH=7,AG=1 |
| B、在25℃时,若溶液呈中性,则pH=7,AG=0 |
| C、在25℃时,岩溶液呈碱性,则pH<7,AG>0 |
| D、在25℃时,若溶液呈酸性,则pH<7,AG<0 |
常温下,下列叙述正确的是( )
| A、中和PH和体积均相同的盐酸和硫酸溶液,消耗NaOH的物质的量之比是1:2 | B、在滴有酚酞的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 | C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 | D、若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 |
对于常温下pH=2的盐酸和pH=3的醋酸,下列说法正确的是( )
| A、pH=2的盐酸中:c(H+)=c(Cl-)+c(OH-) | B、pH=3的醋酸中:c(H+)=3.0mol?L-1 | C、pH=2的盐酸与pH=3的醋酸中溶质的物质的量浓度之比为10:1 | D、pH=3的醋酸与pH=11的NaOH溶液等体积混合所得溶液中:c(Na+)=c(CH3COO-) |