已知在水中的电离方程式为:NaHSO4?Na++H++SO
.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.对于该溶液,下列叙述中不正确的是( )
2- 4 |
| A、该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性 | ||
| B、水电离出来的c(H+)=1×10-10mol?L-1 | ||
C、c(H+)=c(OH-)+c(SO
| ||
| D、该温度高于25℃ |
在100℃时,水的离子积为1×10-12,若该温度下某溶液中H+浓度为1×10-7mol/L,则该溶液①呈碱性 ②呈酸性 ③呈中性 ④c(OH-)=100 c(H+) ( )
| A、① | B、② | C、③④ | D、①④ |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系,下列说法正确的是( )
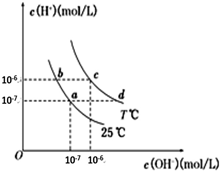

| A、a点对应的溶液和c点对应的溶液pH值大小:pH(c)>pH(a) | B、d点对应的溶液中大量存在:K+、Ba2+、NO3-、I- | C、25℃时,Ka(HF)=3.6×10-4,Ka(CH3COOH)=1.75×10-5,0.1mol/L的NaF溶液与0.1mol/L 的CH3COOK溶液相比:c(Na+)-c(F-)>c(K+)-c(CH3COO-) | D、如b点对应的溶液中只含NaHA,则溶液中粒子浓度大小:c(HA-)>c(H2A)>c(H+)>c(A2-) |
下列有关说法正确的是( )
| A、25℃与60℃时,纯水的pH相等 | B、CaCO3难溶于稀硫酸,也难溶于醋酸 | C、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | D、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 | ||
| B、c (H+)=1.0×10-7 mol/L的溶液 | ||
C、c (H+)=c (O
| ||
| D、pH=3的酸与pH=11碱等体积混合后的溶液 |
下列式子哪一个能用来精确地计算任意稀盐酸溶液中的氢离子浓度c(H+)的是(Kw为水的离子积常数)
( )
( )
| A、c(H+)=c(HCl) | B、c(H+)=c(HCl)-Kw/c(H+) | C、c (H+)=C(HCl)+Kw | D、c(H+)=c(HCl)+Kw/c(H+)) |
常温下,下列离子能使纯水中H+数目增加的是( )
| A、CH3COO- | B、NH4+ | C、HCO3- | D、NO3- |
纯水在90℃和20℃时的PH值分别为M,N,则两者的比较正确的是( )
| A、M<N | B、M=N | C、M>N | D、无法确定 |
加入下列哪种物质或进行哪项操作,不会使水的电离平衡发生移动的是( )
| A、加入NaOH | B、加入CH3COOH | C、加入NaCl | D、升温 |
向纯水中加入少量的NaOH固体(温度不变),则溶液( )
| A、pH值升高 | B、[H+]和[OH-]的乘积增大 | C、显中性 | D、OH-离子浓度减小 |