参考下表中物质的熔点,回答有关问题:
(1)钠的卤化物及碱金属的氯化物的熔点与卤离子及碱金属离子的 有关,随着 的增大,熔点逐渐降低.
(2)硅的卤化物的熔点及硅、锗、锡、铅的氯化物的熔点与 有关,随着 增大, 增强,故熔点逐渐升高.
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与 有关,因为 ,故前者的熔点远高于后者.
| 物质 | 熔点/℃ | 物质 | 熔点/℃ |
| NaF | 993 | SiF4 | -90.2 |
| NaCl | 801 | SiCl4 | -70.4 |
| NaBr | 747 | SiBr4 | 5.2 |
| NaI | 662 | SiI4 | 120.5 |
| NaCl | 801 | SiCl4 | -70.4 |
| KCl | 768 | GeCl4 | -49.5 |
| RbCl | 717 | SnCl4 | -36.2 |
| CsCl | 646 | PbCl4 | -15 |
(2)硅的卤化物的熔点及硅、锗、锡、铅的氯化物的熔点与
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与
在理解概念的基础上,理清概念之间的相互关系,构建知识网络是学习化学的重要方法,如图是中学化学常见化学概念之间的相互关系.
(1)完成下表,且实例按以下要求填写.
①只能由 H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3).
(2)取上述表格中A、B、C三种晶体中某一晶体溶于水得W溶液,写出等物质的量浓度等体积的硫酸氢钠与W溶液反应的离子方程式 ;
(3)写出上述表格中熔点最高的物质与氢氧化钠反应的化学方程式: .

(1)完成下表,且实例按以下要求填写.
①只能由 H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3).
| A | B | C | ||
| 晶体类别 | 金属晶体 | |||
| 实例的化学式 | Na |
(3)写出上述表格中熔点最高的物质与氢氧化钠反应的化学方程式:
有A、B、C三种晶体,分别有H、C、Na、Cl四种元素中的一种或几种形成,对这三种晶体进行实验,结果如下:
(1)晶体的化学式分别为:A、 、B、 C、 .
(2)晶体中微粒间的作用分别为:A、 、B、 C、 .
| 熔点℃ | 硬度 | 水溶性 | 导电性 | 水溶液与Ag+反应 | |
| A | 811 | 较大 | 易溶 | 水溶液(或熔化)导电 | 白色沉淀 |
| B | 3550 | 很大 | 不溶 | 不导电 | 不反应 |
| C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(2)晶体中微粒间的作用分别为:A、
[物质结构与性质]
(1)A、B、C为短周期元素,请根据下表信息回答问题.
①第一电离能:A B(填“>”、“<”或“=”),基态C原子的电子排布式为 .
②B与C由共价键形成的某化合物BC最高可稳定到2200℃,晶体类型为 .
(2)发展煤的液化技术被纳入“十二五”规划,中科院山西煤化所有关煤液化技术的高效催化剂研发项目取得积极进展.已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇(CH3OH)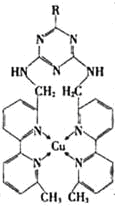 ,从而实现液化.
,从而实现液化.
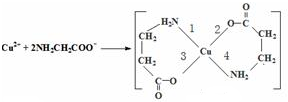
①某含铜的离子结构如图所示,在该离子内部微粒间作用力的类型有 .
a.离子键 b.极性键 c.非极性键 d.配位键 e.范德华力 f.氢键) (填字母)
②煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛(HCHO),甲醇的沸点64.96℃,甲醛的沸点-21℃,甲醇的沸点更高的原因是因为分子间存在着氢键,甲醛分子间没有氢键,但是甲醇和甲醛均易溶于水,原因是它们均可以和水分子间形成氢键.请你说明甲醛分子间没有氢键原因 ;
③甲醇分子中进行sp3杂化的原子有 ;甲醛与H2发生加成反应,当生成1mol甲醇,断裂σ键的数目为 .
0 60538 60546 60552 60556 60562 60564 60568 60574 60576 60582 60588 60592 60594 60598 60604 60606 60612 60616 60618 60622 60624 60628 60630 60632 60633 60634 60636 60637 60638 60640 60642 60646 60648 60652 60654 60658 60664 60666 60672 60676 60678 60682 60688 60694 60696 60702 60706 60708 60714 60718 60724 60732 203614
(1)A、B、C为短周期元素,请根据下表信息回答问题.
| 元素 | A | B | C |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物的水溶液显碱性 | 原子有三个电子层,简单离子在本周期中半径最小 |
②B与C由共价键形成的某化合物BC最高可稳定到2200℃,晶体类型为
(2)发展煤的液化技术被纳入“十二五”规划,中科院山西煤化所有关煤液化技术的高效催化剂研发项目取得积极进展.已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇(CH3OH)
 ,从而实现液化.
,从而实现液化.①某含铜的离子结构如图所示,在该离子内部微粒间作用力的类型有
a.离子键 b.极性键 c.非极性键 d.配位键 e.范德华力 f.氢键) (填字母)
②煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛(HCHO),甲醇的沸点64.96℃,甲醛的沸点-21℃,甲醇的沸点更高的原因是因为分子间存在着氢键,甲醛分子间没有氢键,但是甲醇和甲醛均易溶于水,原因是它们均可以和水分子间形成氢键.请你说明甲醛分子间没有氢键原因
③甲醇分子中进行sp3杂化的原子有
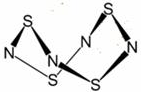 Ⅰ.S4N4的结构如图:
Ⅰ.S4N4的结构如图: