下列变化过程不需要破坏化学键的是( )
| A、碘的升华 | B、铝与强碱溶液反应 | C、食盐溶解于水 | D、氯气溶于水 |
关于含正离子N5+的化合物N5ASF6,下列叙述中错误的是( )
| A、N5+共有34个核外电子 | B、N5+中氮原子间以离子键结合 | C、化合物N5ASF6中AS的化合价为+1价 | D、化合物N5ASF6为离子化合物 |
下列物质在固态时,晶体类型相同的是( )
| A、NH3和H2O | B、NaCl和HCl | C、I2和金刚石 | D、SiO2和CO2 |
下列说法中,正确的是( )
| A、分子间作用力比化学键弱得多 | B、溶液通常是澄清透明的,胶体通常是浑浊的 | C、铁和铜在自然界中只能以化合态形式存在 | D、防止酸雨的最根本途径是减少温室气体的排放 |
 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.则下列说法不正确的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.则下列说法不正确的是( )| A、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl | B、S2Cl2为含有极性键和非极性键的极性分子 | C、S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2 | D、S2Cl2的电子式是 |
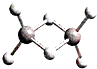 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A、Al2H6可以燃烧,产物为氧化铝和水 | B、1mol Al2H6中约含有4.8×1024个σ键 | C、60g Al2H6中含铝原子约为1.2×1023个 | D、Al2H6在固态时所形成的晶体是离子晶体 |
下列说法正确的是( )
| A、高熔点的固体如果不是离子晶体,则一定为原子晶体 | B、由盐酸的酸性强于氢硫酸的酸性,可推知氧化性:Cl2>S | C、由两种元素组成的共价化合物分子中,只可能存在极性键 | D、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )
| A、CO2和SiO2 | B、CCl4和H2O | C、NaCl和NaOH | D、Na2O2和CaCl2 |
下列关于晶体的说法一定正确的是( )
| A、分子晶体中都存在共价键 | B、在晶体中只要有阴离子,一定有阳离子 | C、在SiO2晶体中,Si原子与Si-O键数目比为1:2 | D、金属晶体的熔点都比分子晶体的熔点高 |
下列说法中正确的是( )
| A、冰融化时,分子中H-O键发生断裂 | B、原子晶体中,共价键越强,熔点越高 | C、分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高 | D、熔融状态下能导电的物质一定是离子化合物 |