题目内容
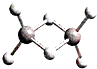 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A、Al2H6可以燃烧,产物为氧化铝和水 | B、1mol Al2H6中约含有4.8×1024个σ键 | C、60g Al2H6中含铝原子约为1.2×1023个 | D、Al2H6在固态时所形成的晶体是离子晶体 |
分析:A.Al2H6作高能燃料可以燃烧根据原子个数守恒判断产物;
B.1mol Al2H6中含有6molAl-H键和1molAl-Alσ键,据此解答;
C.1molAl2H6中含有2molAl,求出60gAl2H6的物质的量,就可求其所含Al的个数;
D.分子晶体熔沸点比较低,离子晶体熔沸点高,根据熔沸点可以判断时分子晶体.
B.1mol Al2H6中含有6molAl-H键和1molAl-Alσ键,据此解答;
C.1molAl2H6中含有2molAl,求出60gAl2H6的物质的量,就可求其所含Al的个数;
D.分子晶体熔沸点比较低,离子晶体熔沸点高,根据熔沸点可以判断时分子晶体.
解答:解:A.Al2H6 燃烧的方程式:Al2H6+O2
Al2O3+H2O,故A正确;
B.1mol Al2H6中含有6molAl-H键和1molAl-Alσ键,所含Al-Alσ键的个数:1mol×NA=6.02×1023个,故B错误;
C.Al2H6的摩尔质量为:60g/mol,所以60gAl2H6的物质的量是1mol,1molAl2H6中含有2molAl,所以60g该物质中含Al个数2NA,约为1.2×1024个,故C错误;
D.Al2H6的熔点为150℃,熔点低,所以可以判断该物质在固体时是分子晶体,故D错误;
故选A.
| ||
B.1mol Al2H6中含有6molAl-H键和1molAl-Alσ键,所含Al-Alσ键的个数:1mol×NA=6.02×1023个,故B错误;
C.Al2H6的摩尔质量为:60g/mol,所以60gAl2H6的物质的量是1mol,1molAl2H6中含有2molAl,所以60g该物质中含Al个数2NA,约为1.2×1024个,故C错误;
D.Al2H6的熔点为150℃,熔点低,所以可以判断该物质在固体时是分子晶体,故D错误;
故选A.
点评:本题考查了氢铝化合物的结构和性质,该物质平时接触少,所以对其结构性质了解少,题目难度比较大,解题时注意认真审题仔细分析其结构.

练习册系列答案
相关题目
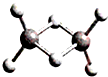 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、Al2H6在空气中完全燃烧,产物为氧化铝和水 | C、氢铝化合物可能成为未来的储氢材料和火箭燃料 | D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
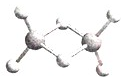 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、氢铝化合物可能成为未来的储氢材料和火箭燃料 | C、Al2H6在空气中完全燃烧,产物为氧化铝和水 | D、Al2H6中含有离子键和极性共价键 |
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量。Al2H6球棍模型如下图。下列说法肯定错误的是( )
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |
