下列晶体中存在单个分子的是( )
| A、白磷 | B、氯化钠 | C、金刚石 | D、二氧化硅? |
下列各式能真实表示物质分子组成的是( )
| A、CaF2 | B、CH4 | C、SiO2 | D、Na2O2 |
下面关于晶体的叙述中,错误的是( )
| A、氯化铯晶体中,每个Cs+周围紧邻8个Cl- | B、氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个 | C、干冰晶体中,每个CO2分子周围紧邻12个CO2分子 | D、金刚石为网状结构,由共价键形成的碳原子环中,最小环上有6个碳原子 |
下列宝石中,被誉为“硬度之王”的是( )
| A、珍珠 | B、钻石 | C、红宝石 | D、蓝宝石 |
下列关于晶体的叙述中,错误的是( )
| A、每1molSi晶体中,含有2molSi-Si共价键 | B、在CO2晶体中,与每个CO2分子周围紧邻的有12个CO2分子 | C、在CsCl晶体中,与每个Cs+周围紧邻的有8个Cl-,而与每个Cs+等距离紧邻的也有8个Cs+ | D、在简单立方堆积的金属晶体中,每个金属原子周围紧邻的有6个金属原子 |
下列有关晶体的叙述中,错误的是( )
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | B、白磷分子晶体中,微粒之间通过共价键结合,键角为60° | C、在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+) | D、离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键不被破坏 |
美国Lawrece Liermore国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体说法,正确的是( )
| A、CO2的原子晶体和分子晶体互为同分异构体 | B、在一定条件下,CO2原子晶体转化为CO2分子晶体是物理变化 | C、CO2的原子晶体和CO2分子晶体具有相同的物理性质和化学性质 | D、在CO2的原子晶体中,每一个C原子结合4个O原子,每一个O原子跟两个C原子相结合 |
下列有关晶体的叙述中,错误的是( )
| A、在SiO2晶体中,每个Si原子与4个O原子形成共价键 | B、在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 | C、NaCl晶体中与每个Na+距离相等且最近的Cl-有6个 | D、CsCl晶体中与每个Cs+距离相等且最近的Cl-有8个 |
下列说法一定正确的是( )
| A、位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的最高化合价X<Y | B、PH=2盐酸和醋酸溶液各10ml,分别加水稀释到1L,所得溶液的pH较小的是醋酸 | C、二氧化硅晶体中,每个硅原子与2个氧原子形成共价键 | D、在晶体中只要有阳离子就一定有阴离子 |
水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为 ;
(2)H2O分子中氧原子采取的是 杂化.写出与H2O分子互为等电子体的微粒 .(写一个即可)
(3)水分子容易得到一个H+形成水合氢离子(H3O+).对上述过程的下列描述不合理的是 .
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.水分子仍保留它的化学性质 D.微粒中的键角发生了改变
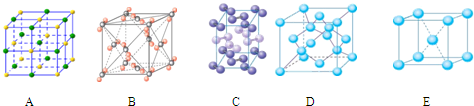
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序).与冰的晶体
类型相同的是 (请用相应的编号填写)
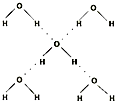
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”是 kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.请写出生成此配合离子的离子方程式: .
(7)已知下列元素的电负性数据:H:2.1,O:3.5,F:4.0.OF2与水的立体结构相似,但水分子的极性比OF2强得多,其原因有:①OF2中氧原子上有两对孤对电子,抵消了F一O键中共用电子对偏向F而产生的极性;②从电负性上看,
(8)分析下表数据,请写出你的最具概括性的结论:
① ;② .
0 60519 60527 60533 60537 60543 60545 60549 60555 60557 60563 60569 60573 60575 60579 60585 60587 60593 60597 60599 60603 60605 60609 60611 60613 60614 60615 60617 60618 60619 60621 60623 60627 60629 60633 60635 60639 60645 60647 60653 60657 60659 60663 60669 60675 60677 60683 60687 60689 60695 60699 60705 60713 203614
(1)水分子中氧原子在基态时核外电子排布式为
(2)H2O分子中氧原子采取的是
(3)水分子容易得到一个H+形成水合氢离子(H3O+).对上述过程的下列描述不合理的是
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.水分子仍保留它的化学性质 D.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序).与冰的晶体
类型相同的是


(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”是
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.请写出生成此配合离子的离子方程式:
(7)已知下列元素的电负性数据:H:2.1,O:3.5,F:4.0.OF2与水的立体结构相似,但水分子的极性比OF2强得多,其原因有:①OF2中氧原子上有两对孤对电子,抵消了F一O键中共用电子对偏向F而产生的极性;②从电负性上看,
(8)分析下表数据,请写出你的最具概括性的结论:
| 键型 | 键能 (kJ/mol) |
键长 (pm) |
分子 | 键角 | 物质 | 熔点(℃) | 沸点(℃) |
| H-C | 413 | 109 | 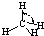 |
109.5° | 甲烷 | -183.7 | -128.0 |
| H-N | 391 | 101 | 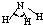 |
107° | 氨 | -77.7 | -33.3 |
| H-O | 467 | 96 | 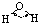 |
104.5° | 水 | 0.0 | 100.0 |