有关乙炔分子中的化学键描述不正确的是( )
| A、两个碳原子采用sp杂化方式 | B、两个碳原子采用sp2杂化方式 | C、每个碳原子都有两个未杂化的2p轨道形成π键 | D、两个碳原子形成两个π键 |
下列分子中的中心原子杂化轨道的类型和分子构型都相同的是( )
| A、CO2与SO2 | B、NH3与BF3 | C、CH4与NH4+ | D、C2H2与C2H4 |
了解有机物分子中化学键特征以及成键方式是研究有机物性质的重要基础.下列关于有机物分子的成键方式的描述不正确的是( )
| A、烷烃分子中碳原子均采用sp3杂化成键 | B、苯分子中碳原子间是以σ键和π键交替连接 | C、苯乙烯分子中所有碳原子均采用sp2杂化成键 | D、苯环中存在6个碳原子共有的大π键 |
在以下的分子或离子中,空间结构的几何形状是三角锥形的是( )
| A、SO42- | B、CH4 | C、CO2 | D、NF3 |
下列描述中正确的是( )
| A、CS2为V形的极性分子 | ||
B、ClO
| ||
| C、SiH4的沸点高于CH4,可推测PH3的沸点高于NH3 | ||
| D、SiF4和SO2-3的中心原子均为sp3杂化 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A、两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 | B、NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 | C、NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 | D、氨气分子是极性分子而甲烷是非极性分子 |
三氟化硼(BF3)是一种无色气体,用于制造火箭的高能燃料.已知BF3是非极性分子,下列描述正确的是( )
| A、BF3分子呈三角锥形 | B、BF3沸点低于BCl3 | C、B-F键键能低于B-Cl键 | D、F-B-F间的夹角为109°28′ |
有四种物质:①金刚石;②白磷;③甲烷;④石墨,其中具有正四面体结构的是( )
| A、①②③ | B、①③④ | C、①② | D、②③ |
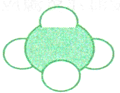 如图是某物质分子的比例模型,该物质的分子式是( )
如图是某物质分子的比例模型,该物质的分子式是( )| A、NH3 | B、CH4 | C、H2O | D、C2H4 |
 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A、该物质中氮元素有两种不同的化合价 | B、该物质可以归类于亚硝酸盐类化合物 | C、该分子中的4个氮原子构成正四面体 | D、该分子中氮原子的化学环境各不相同 |