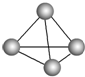
 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量,根据以上信息和数据,下列说法正确的是( )| A、N4属于一种新型的化合物 | B、N4分子是非极性分子 | C、N4沸点比P4(白磷)高 | D、0.1molN4气体转变为N2将放出882kJ热量 |
根据已知条件,对物质的性质强弱判断不正确的是( )
| A、已知HF的共价键键能比HCl大,说明稳定性:HF>HCl | ||||
| B、已知正反应的活化能大于逆反应的活化能,说明总能量:生成物>反应物 | ||||
C、已知 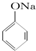 +SO2+H2O→ +SO2+H2O→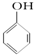 +Na2SO3,说明给出质子能力:HSO3->苯酚 +Na2SO3,说明给出质子能力:HSO3->苯酚 | ||||
D、已知CaCO3+SiO2
|
下列说法不正确的是( )
| A、键角是描述分子立体结构的重要参数,键长是形成共价键的两原子间的核间距 | B、杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 | C、分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 | D、质谱能够快速、微量、精确的测定有机物相对分子质量 |
下列现象能用键能大小解释的是( )
| A、稀有气体一般很难发生化学反应 | B、常温常压下,溴呈液态 | C、氮气的化学性质比氧气稳定 | D、硝酸容易挥发,而硫酸很难挥发 |
下列叙述正确的是( )
| A、Cl-Cl、Br-Br、I-I的键长逐渐增大,键能也逐渐增大 | B、碘的晶体中碘分子之间的范德华力小于氯的晶体中氯分子之间的范德华力 | C、H2SO4、H3PO4、HClO4的酸性依次减弱 | D、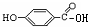 的沸点比 的沸点比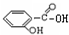 的沸点高 的沸点高 |
HCl分子中氢氯键(H-Cl)的键能大约是HCl分子间范德华力的( )倍.
| A、20 | B、2 | C、0.5 | D、0.05 |
PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低.下列判断错误的是( )
| A、PH3分子呈三角锥形 | B、PH3分子是极性分子 | C、PH3沸点低于NH3沸点,因为P-H键键能低 | D、PH3分子稳定性低于NH3分子,因为N-H键键能高 |
在1molP原子形成的白磷中含有P-P键为(NA为阿氏常数)( )
| A、3NA | B、1.5 NA | C、4 NA | D、0.25 NA |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、124g P4含有P-P键的个数为4NA | B、12g石墨中含有C-C键的个数为NA | C、12g金刚石中含有C-C键的个数为2NA | D、60g Si02中含Si-O键的个数为2NA |
化学家若合成了一种寓有“爱你一生一世”之意的链状烃.该烃的化学式为C2013H2014,并含有多个碳碳叁键.则该分子中含-C≡C-的数目最多不能超过( )
| A、501 | B、503 | C、505 | D、507 |