题目内容
根据已知条件,对物质的性质强弱判断不正确的是( )
| A、已知HF的共价键键能比HCl大,说明稳定性:HF>HCl | ||||
| B、已知正反应的活化能大于逆反应的活化能,说明总能量:生成物>反应物 | ||||
C、已知 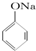 +SO2+H2O→ +SO2+H2O→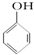 +Na2SO3,说明给出质子能力:HSO3->苯酚 +Na2SO3,说明给出质子能力:HSO3->苯酚 | ||||
D、已知CaCO3+SiO2
|
分析:A、共价键键能越大,共价键越强,化合物越稳定;
B、吸热反应的正反应的活化能大于逆反应的活化能;
C、根据较强酸制较弱酸、较弱酸不能制较强酸分析;
D、碳的非金属性大于硅.
B、吸热反应的正反应的活化能大于逆反应的活化能;
C、根据较强酸制较弱酸、较弱酸不能制较强酸分析;
D、碳的非金属性大于硅.
解答:解:A、共价化学物的稳定性取决于共价键的强弱,共价键键能越大,共价键越强,化合物越稳定,故A正确;
B、吸热反应的正反应的活化能大于逆反应的活化能,生成物的总能量大于反应物的总能量为吸热反应,故B正确;
C、 +SO2+H2O→
+SO2+H2O→ +Na2SO3,说明亚硫酸的酸性大于苯酚的酸性,苯酚和Na2SO3不反应说明HSO3-的酸性大于苯酚的酸性,因此给出质子能力:HSO3->苯酚,故C正确;
+Na2SO3,说明亚硫酸的酸性大于苯酚的酸性,苯酚和Na2SO3不反应说明HSO3-的酸性大于苯酚的酸性,因此给出质子能力:HSO3->苯酚,故C正确;
D、碳的非金属性大于硅,CaCO3+SiO2
CaSiO3+CO2↑不能用于判断C和Si的非金属性的强弱,故D错误;
故选:D.
B、吸热反应的正反应的活化能大于逆反应的活化能,生成物的总能量大于反应物的总能量为吸热反应,故B正确;
C、
 +SO2+H2O→
+SO2+H2O→ +Na2SO3,说明亚硫酸的酸性大于苯酚的酸性,苯酚和Na2SO3不反应说明HSO3-的酸性大于苯酚的酸性,因此给出质子能力:HSO3->苯酚,故C正确;
+Na2SO3,说明亚硫酸的酸性大于苯酚的酸性,苯酚和Na2SO3不反应说明HSO3-的酸性大于苯酚的酸性,因此给出质子能力:HSO3->苯酚,故C正确;D、碳的非金属性大于硅,CaCO3+SiO2
| ||
故选:D.
点评:本题考查了键能、活化能、非金属性的判断和应用,涉及“较强酸制较弱酸、较弱酸不能制较强酸”的经验规律,题目难度中等,注意基础知识的掌握和应用.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目

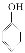

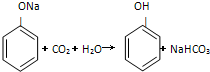
 Si+2CO↑,说明非金属性:碳>硅
Si+2CO↑,说明非金属性:碳>硅 ,说明酸性:碳酸>苯酚
,说明酸性:碳酸>苯酚