下列分子中各元素原子最外层电子全部参与成键的是( )
| A、HF | B、CO2 | C、CH4 | D、Cl2 |
下列各分子中,所有原子都满足最外层为8电子结构的是( )
①H2O、②BF3、③CCl4、④PCl5、⑤XeF4、⑥CO2、⑦BeCl2、⑧Mg3N2、⑨PCl3、⑩CO.
①H2O、②BF3、③CCl4、④PCl5、⑤XeF4、⑥CO2、⑦BeCl2、⑧Mg3N2、⑨PCl3、⑩CO.
| A、①③⑥⑧⑨ | B、②③⑥⑧⑨ | C、③⑥⑧⑨ | D、③④⑥⑦⑧⑨⑩ |
下列有关原子轨道的能量或个数的说法正确的是( )
| A、3d表示有3个d轨道 | B、同一原子中,原子轨道的能量:4s>3p | C、同一原子中,形状相同的原子轨道的能量相同 | D、同一原子中,电子层相同的原子轨道的能量相同 |
下列化学用语中不正确的是( )
| A、钠原子的电子排布式为:1s22s22p63s1 | B、Fe3+的电子排布式为:[Ar]3d5 | C、磷原子的核外电子排布图: | D、硅原子的核外电子排布图: |
下列微粒中,未成对电子数最多的是( )
| A、O:1s22s22p4 | B、P:1s22s22p63s23p3 | C、Cr:1s22s22p63s23p63d54s1 | D、Mn:1s22s22p63s23p63d54s2 |
主族元素M、R形成的简单离子M2-离子与R+离子的核外电子数之和为20,下列说法正确的是( )
| A、M原子的质子数一定大于R原子的质子数 | B、M可能存在16M、18M两种核素 | C、M2-的离子与R+的电子层结构不可能相同 | D、两种离子结合形成的化合物中可能含有共价键 |
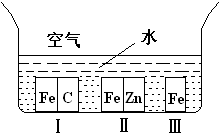 A、【供选学《化学与生活》考生作答】
A、【供选学《化学与生活》考生作答】(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是
(2)氟氯代烷是一种破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2;②O3→O+O2;③ClO→Cl+O2
上列反应的总反应式是
(3)碳酸氢钠是常见的疏松剂,主要是因为它在加热条件下产生了气体,使食品变得疏松.试写出碳酸氢钠受热分解的化学方程式
(4)垃圾资源化的方法是
A、填埋 B、焚烧 C、堆肥法 D、分类回收法
B【供选学《化学反应原理》考生作答】
设反应①Fe(s)+CO2(g)═FeO(s)+CO(g)的平衡常数为K1.反应②Fe(s)+H2O(g)═FeO(s)+H2(g)的平衡常数K2,在不同温度下,K1、K2的值如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③CO2(g)+H2(g)═CO(g)+H2O(g)写出该反应的平衡常数K3的数学表达式:K3═
(3)书写热化学方程式:
①1mol N2(g)与适量O2(g)起反应,生成NO2(g),吸收68KJ热量:
②NH3(g)燃烧生成NO2(g)和H2O(g),已知
(1)2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol
(2)N2(g)+2O2(g)═2NO2(g)△H═+67.8kJ/mol
1,N2(g)+3H2(g)═2NH3(g)△H═-92.0kJ/mol
NH3(g)燃烧生成NO2(g)和H2O (g)热化学方程式:
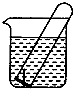 (1)如图所示,水槽中试管内有一枚铁钉,放置数天观察:铁钉在逐渐生锈.若试管内液面上升,发生
(1)如图所示,水槽中试管内有一枚铁钉,放置数天观察:铁钉在逐渐生锈.若试管内液面上升,发生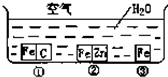 如何防止铁的锈蚀是工业上研究的重点内容.为研究铁的锈蚀,如下图所示,铁处于①、②、③三种不同的环境中.请回答:
如何防止铁的锈蚀是工业上研究的重点内容.为研究铁的锈蚀,如下图所示,铁处于①、②、③三种不同的环境中.请回答: