时刻向密闭容器中加入A、B、C三种气体,保持一定温度,在t1、t2、t3、t4各时刻测得各物质的浓度如表所示.据此推断以下各说法中不正确的是( )
| 测定时刻/s | t1 | t2 | t3 | t4 |
| c(A)/mol?L- | 6 | 3 | 2 | 2 |
| c(B)/mol?L- | 5 | 3.5 | 3 | 3 |
| c(C)/mol?L- | 1 | 2.5 | 3 | 3 |
| A、在t3时刻反应已经停止 | ||
| B、达到平衡时A的转化率比B的转化率大 | ||
| C、在容器内发生的反应为2A+B?C | ||
D、在t2~t3时间段内A的平均反应速率为
|
在一定条件下存在反应:I2(g)+H2(g)?2HI(g),其正反应放热.现有3个相同的2L恒容绝热(与外界没有热量交换)密闭容器甲、乙、丙,在甲中充入1mol I2(g)和1mol H2(g),在乙中充入2mol HI(g),在丙中充入2mol I2(g)和2mol H2(g),在一定温度下下开始反应.达到平衡时,下列说法不正确的是( )
| A、容器甲、丙中,逆反应的速率:v(甲)=v(丙) | B、容器甲、乙中,HI 的物质的量:n(甲)<n(乙) | C、容器甲、乙中有关反应物的转化率:α(H2)+α(HI)<100% | D、容器甲、乙中,化学平衡常数:K(甲)=K(乙) |
某温度下,在容积为2L的密闭容器中加入物质A(g),发生反应:xA(g)?B(g)+C(g)△H>0
在不同时间,测得容器中各物质的物质的量如表所示:
下列说法正确的是( )
在不同时间,测得容器中各物质的物质的量如表所示:
| 0s | 20s | 40s | 60s | |
| n(A)/mol | a | 3.0 | 2.0 | 2.0 |
| n(B)/mol | 0 | 1.0 | 2.0 | c |
| n(C)/mol | 0 | 1.0 | b | 2.0 |
| A、反应在前20s内的平均速率为v(A)=0.05 mol?L-1?s-1 |
| B、40s时,反应的正反应速率和逆反应速率相等 |
| C、该温度下,反应的化学平衡常数为1 |
| D、若升高温度,则化学平衡常数减小 |
一定温度下,某密闭容器中发生反应:2HI(g)?H2(g)+I2(g)△H>0,若15s内c(HI)由0.1mol?L-1降到0.07mol?L-1,则下列说法正确的是( )
| A、15s内用H2表示的平均反应速率为v(H2)=0.002mol?L-1?s-1 | B、升高温度平衡逆向移动 | C、c(HI)由0.07mol?L-1降到0.05mol?L-1所需时间为10s | D、减小反应体系的体积,化学反应速率加快 |
 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图.则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图.则图中阴影部分的面积表示( )| A、X的浓度的变化 | B、Y的物质的量的变化 | C、Z的浓度的变化 | D、Z的物质的量的减少 |
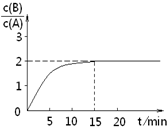 已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:
已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g)═B(g)+C(g);△H=-48.25kJ?mol-1
反应过程中时间t与A、B浓度有如图关系,若测得第15min时
c(B)=1.6mol?L-1,则下列结论正确的是( )
| A、反应在前15min的平均速率ν(A)=0.11 mol?L-1?min-1 | B、A的初始物质的量为8 mol | C、反应到达平衡的过程中,放出的热量是77.2kJ | D、如使反应最终c(B)/c(A)=1.5,恒温恒容时,加入一定量的A可以实现 |
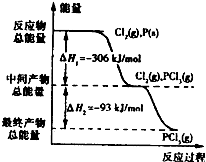 如图是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程和能量关系图.其中PCl5(g)分解成PCl3(g)和Cl2(g)的反应是一个可逆反应,温度T℃时,在密闭容器中加入0.6mol PCl5,达平衡时,PCl5还剩0.45mol,其分解率为α,则下列推断不正确的是( )
如图是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程和能量关系图.其中PCl5(g)分解成PCl3(g)和Cl2(g)的反应是一个可逆反应,温度T℃时,在密闭容器中加入0.6mol PCl5,达平衡时,PCl5还剩0.45mol,其分解率为α,则下列推断不正确的是( )| A、α等于25% | B、若升高温度,平衡时PCl5的分解率小于α | C、若初始时加入0.6mol PCl3和0.6 mol Cl2,以相同条件进行反应,则平衡时PCl3转化率为3α | D、PCl5分解的热化学方程式为:PCl5(g)?PCl3(g)+Cl2(g)△H=-93kJ?mol-1 |
某温度下,H2(g)+CO2(g)
H2O(g)+CO(g) (△H>0)的平衡常数K=
,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:下列判断有错的是( )
| △ |
| 9 |
| 4 |
| 起始浓度(mol/L) | 甲 | 乙 | 丙 | 丁 |
| c(H2) | 0.01 | 0.02 | 0.02 | 0.005 |
| c(CO2) | 0.01 | 0.01 | 0.02 | 0.005 |
| c(H2O) | 0 | 0 | 0 | 0.005 |
| c(CO) | 0 | 0 | 0 | 0.005 |
| A、平衡时,乙中CO2的转化率>60% | ||
B、平衡时,四容器中甲的
| ||
| C、起始时丁向正反应方向进行 | ||
| D、反应开始时,丙中反应速率最快 |
 在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )A、平衡常数K=
| ||
| B、该反应在T1时的平衡常数比T2时的小 | ||
C、任意时刻,T2温度下的反应速率均大于T1温度下的速率
| ||
| D、处于A点的反应体系从T1变到T2,达到平衡时增大 |



