某化学研究小组探究外界条件对化学反应mA(g)+nB(g)?pC(g)的速率和平衡的影响图象如下,下列判断正确的是( )
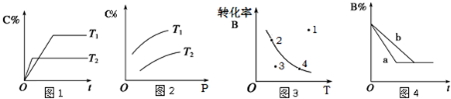

| A、由图1可知,T1<T2,该反应正反应为吸热反应 | B、由图2可知,该反应m+n<p | C、图3中,表示反应速率v正>v逆的是点3 | D、图4中,若m+n=p,则a曲线一定使用了催化剂 |
同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/mol.测得数据如表
下列叙述不正确的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| (1) | 2 | 3 | 0 | 27.78kJ |
| (2) | 1.6 | 1.8 | 0.8 | Q |
| A、容器(1)(2)反应达平衡时压强相等 |
| B、容器(2)中反应开始时v(正)>v(逆) |
| C、容器(2)中反应达平衡时,吸收的热量Q为9.26kJ |
| D、若条件为“绝热恒容”,容器(1)中反应达平衡时n(NH3)<0.6mol |
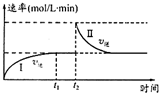 在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图.下列说法正确的是( )
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图.下列说法正确的是( )| A、0~t2时,v正>v逆 | B、Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ | C、t2时刻改变的条件可以是向密闭容器中加C | D、Ⅰ、Ⅱ两过程达到平衡时,平衡常数I<Ⅱ |
在密闭容器中进行反应X2(g)+3Y2(g)?2Z2(g),若X2、Y2、Z2的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,达到平衡时下列物质的浓度不可能为( )
| A、X2为0.3mol/L | B、Y2为0.2mol/L | C、Z2为0.35mol/L | D、Y2为0.6mol/L |
下列关于可逆反应的叙述不正确的是( )
| A、可逆反应是指在相同条件下,既能向正方向进行同时又能向逆方向进行的反应. | B、可逆反应在一定条件下可达到平衡状态,该状态下,正、逆反应速率相等 | C、可逆反应不能进行到底,必然有反应物剩余 | D、可逆反应的速率都很小,达平衡时反应停止 |
在密闭容器中有如下反应:2A(g)+O2(g)?2B(g),已知反应过程中某一时刻A、O2、B的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
| A、A为0.4mol/L、O2为0.2mol/L | B、A为0.25mol/L | C、A、B均为0.15mol/L | D、B为0.4mol/L |
在一定条件下,向2L密闭容器中充入3mol X气体和1mol Y气体发生下列反应:2X(g)+Y(g)?3Z(g)+2W(g),在某一时刻达到化学平衡时,测出的下列各生成物浓度的数据肯定错误的是( )
| A、c(Z)=0.75mol?L-1 | B、c(Z)=1.20mol?L-1 | C、c(W)=0.80mol?L-1 | D、c(W)=1.00mol?L-1 |
下列反应中不属于可逆反应的是( )
| A、2NO2?N2O4 | |||
B、N2+3H2
| |||
| C、Cl2+H2O?HCl+HClO | |||
D、Pb+PbO2+2H2SO4
|
将2molS02和2molO2放入一个容器中,在一定的条件下反应到达平衡状态,此时,容器存在的各物质的量中,下列可能存在的是( )
| A、0molS02 | B、2mol S03 | C、1mol 02 | D、1molSO3 |