H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-a kJ?mol-1
已知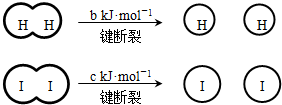 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
已知
 (a、b、c均大于零)
(a、b、c均大于零)下列说法不正确的是( )
| A、反应物的总能量高于生成物的总能量 | B、断开1mol H-H键和1mol I-I键所需能量大于断开2mol H-I键所需能量 | C、断开2mol H-I键所需能量约为(c+b+a)kJ | D、向密闭容器中加入2mol H2和2mol I2,充分反应后放出的热量小于2a kJ |
已知:H2(g)+F2(g)=2HF(g)△H=-270kJ/mol,下列说法正确的是( )
| A、在相同条件下,1mol H2与1mol F2的能量总和大于2mol HF气体的能量 | B、1mol H2与1mol F2反应生成2mol液态HF放出的热量小于270kJ | C、该反应的逆反应是放热反应 | D、该反应过程的能量变化可用如图来表示 |
有关能量的判断或表示方法正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | B、从C(石墨)═C(金刚石)△H=+1.19kJ?mol-1,可知:金刚石比石墨更稳定 | C、由H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1,可知:含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出热量大于57.3kJ | D、2g H2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ?mol-1 |
下列说法中正确的是( )
| A、1 mol强酸与1mol强碱发生中和反应所放出的热量叫做中和热 | B、铝粉与氧化铁粉末反应中生成物总能量高于反应物总能量 | C、H2S的热稳定性小于H2O是由于H2S分子间不存在氢键 | D、原子晶体中的各相邻原子间都以共价键相结合 |
H2(g)+Cl2(g)═2HCl(g)反应的能量变化示意图如图所示,下列说法错误的是( )

| A、1mol H-H键断裂需要吸收436kJ的能量 | B、相同条件下H2比Cl2稳定 | C、该反应的热化学方程式是H2(g)+Cl2(g)═2HCl(g)△H=+248kJ/mol | D、1mol H2(g)和1mol Cl2(g)的总能量高于2mol HCl(g)的总能量 |
下列关于反应过程中能量变化的说法正确的是( )


| A、在一定条件下,某可逆反应的△H=+100kJ?mol-1,则该反应正反应活化能比逆反应活化能大100kJ?mol-1 | B、图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0未使用和使用催化剂时,反应过程中的能量变化 | C、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | D、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2 |
下列说法正确的是( )
| A、一定温度压强下,△H<0、△S>0的反应一定能自发进行 | B、铅蓄电池放电时的负极和充电时的阴极均发生还原反应 | C、为保护浸入海水中的钢闸门,可将闸门连接到直流电源的正极上 | D、一定温度下,反应:2A(g)+B(g)?2C(g),增大压强反应速率加快,A的浓度减小 |
常温下,1mol化学键分解成气态原子所需要的能量用E表示.根据表中信息判断下列说法不正确的是( )
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ?mol-1) | 436 | 157 | 568 | 432 | 298 |
| A、432 kJ?mol-1>E(H-Br)>298 kJ?mol-1 |
| B、表中最稳定的共价键是H-F键 |
| C、H2(g)→2H (g)?△H=+436 kJ?mol-1 |
| D、H2(g)+F2(g)=2HF(g)?△H=-25 kJ?mol-1 |
下列说法中正确的是( )
| A、熵增加且放热的反应一定是自发反应 | B、自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 | C、凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 | D、非自发反应在任何条件下都不能发生 |
 目前有人提出理想的氢能源循环体系,类似于光合作用,太阳能和水是取之不尽、用之不竭,而且价格低廉的重要资源.按照如图所示的循
目前有人提出理想的氢能源循环体系,类似于光合作用,太阳能和水是取之不尽、用之不竭,而且价格低廉的重要资源.按照如图所示的循环关系,急需化学家研究和解决的是( )
| A、制备大量燃料电池 | B、研发氢氧发电机 | C、将海水提纯 | D、研发合适光分解催化剂,使之在光照下促进水的分解速率加快 |