A、B、C为短周期元素,在周期表中如表所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法不正确的是( )
| A | D | C |
| B |
| A、A的氧化物有多种形式 |
| B、B的最高价氧化物对应的水化物是一种强酸 |
| C、C的氢化物水溶液通常用玻璃试剂瓶盛放 |
| D、D元素形成的单质不止一种 |
现在,含有元素硒(Se)的保健品已开始进入市场.已知它与氧同族,与钾同周期.则下列关于硒的叙述中,不正确的是( )
| A、非金属性比硫强 | B、最高价氧化物的化学式是SeO3 | C、硒是半导体 | D、气态氢化物的化学式为H2Se |
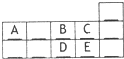 如表为元素周期表中短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
如表为元素周期表中短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )| A、元素原子的半径由大到小的顺序是:D>E>A>B>C | B、元素D的最高价氧化物对应水化物的酸性最强 | C、元素D的单质在过量的B2中充分燃烧的主要产物为DB3 | D、元素B是形成化合物最多的元素 |
下列叙述中正确的是( )
| A、Na原子失电子能力比Mg原子强 | B、氟的氢化物不稳定 | C、H2SO4比H3PO4酸性弱 | D、Mg(OH)2比Ba(OH)2的碱性强 |
如图是元素周期表中短周期的一部分,若a原子最外层电子数比次外层少3,则下列说法正确的是( )
| d | ||
| a | b | c |
| A、a、b、c的最高价氧化物对应水化化物的酸性强弱关系是c>b>a |
| B、d的氢化物没有b的氢化物稳定 |
| C、原子半径的大小关系c>b>a |
| D、单质的氧化性关系:a>b |
下列各组顺序的排列不正确的是( )
| A、金属性:Na<Mg<Al | B、热稳定性:HCl>H2S>PH3 | C、酸性强弱:H4SiO4<H2CO3<HNO3 | D、原子半径大小:Na>S>O |
短周期元素X、Y、Z在周期表中位置如图.下列说法正确的是( )
| Z | |
| X | Y |
| A、若它们均为金属元素,则X与氧元素组成的物质有多种 |
| B、若它们的原子最外层电子数之和为11,则它们均为非金属元素 |
| C、Z单质一定不能置换出Y单质 |
| D、Z元素的最高化合价一定等于Y元素 |
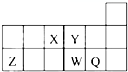 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )| A、元素Y最高正化合价与最低负化合价的绝对值之和的数值等于8 | B、原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q) | C、离子Y2-和Z3+半径的大小顺序为:r(Y2-)>r(Z3+) | D、元素W的最高价氧化物对应的水化物的酸性比Q的强 |
下列说法正确的是( )
| A、Li、Na、K元素的原子核外电子层数随着核电荷数的增加而减少 | B、第二周期元素从Li到F,非金属性逐渐减弱 | C、因为K比Na容易失去电子,所以K比Na的还原性强 | D、O与S为同主族元素,且O比S的非金属性弱 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法不合理的是( )
| A、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y | B、因为酸性H2SO3>H2CO3,所以非金属性S>C | C、硅、锗都位于金属与非金属的交界处,都可以做半导体材料 | D、Ca和Ba分别位于第ⅡA族第四周期和第六周期,则碱性:Ca(OH)2<Ba(OH)2 |