籾朕坪否
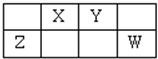
泌夕頁圷殆巓豚燕嶄玉巓豚議匯何蛍⇧飛a圻徨恷翌蚊窮徨方曳肝翌蚊富3⇧夸和双傍隈屎鳩議頁↙ ⇄
| d | ||
| a | b | c |
| A、a、b、c議恷互勺剳晒麗斤哘邦晒晒麗議磨來膿樋購狼頁c﹅b﹅a |
| B、d議狽晒麗短嗤b議狽晒麗糧協 |
| C、圻徨磯抄議寄弌購狼c﹅b﹅a |
| D、汽嵎議剳晒來購狼⦿a﹅b |
蛍裂⦿喇圷殆壓巓豚燕嶄議了崔辛岑⇧d了噐及屈巓豚⇧a、b、c了噐及眉巓豚⇧a圻徨恷翌蚊窮徨方曳肝翌蚊窮徨方富3倖⇧絞a圻徨恷翌蚊窮徨方葎5⇧夸a葎P圷殆⇧絞b葎S圷殆⇧c葎Cl圷殆⇧d葎O圷殆⇧
A⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧掲署奉來埆膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來埆膿◉
B⤴揖麼怛徭貧遇和掲署奉來受樋⇧掲署奉來埆膿⇧狽晒麗埆糧協◉
C⤴揖巓豚徭恣遇嘔圻徨磯抄受弌◉
D⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧汽嵎議剳晒來奐膿⤴
A⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧掲署奉來埆膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來埆膿◉
B⤴揖麼怛徭貧遇和掲署奉來受樋⇧掲署奉來埆膿⇧狽晒麗埆糧協◉
C⤴揖巓豚徭恣遇嘔圻徨磯抄受弌◉
D⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧汽嵎議剳晒來奐膿⤴
盾基⦿盾⦿喇圷殆壓巓豚燕嶄議了崔辛岑⇧d了噐及屈巓豚⇧a、b、c了噐及眉巓豚⇧a圻徨恷翌蚊窮徨方曳肝翌蚊窮徨方富3倖⇧絞a圻徨恷翌蚊窮徨方葎5⇧夸a葎P圷殆⇧絞b葎S圷殆⇧c葎Cl圷殆⇧d葎O圷殆⇧
A⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來奐膿⇧絞A屎鳩◉
B⤴揖麼怛徭貧遇和掲署奉來受樋⇧狽晒麗糧協來受樋⇧絞B危列◉
C⤴揖巓豚徭恣遇嘔圻徨磯抄受弌⇧絞圻徨磯抄a﹅b﹅c⇧絞C危列◉
D⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧汽嵎議剳晒來奐膿⇧絞剳晒來a〽b⇧絞D危列⇧
絞僉A⤴
A⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來奐膿⇧絞A屎鳩◉
B⤴揖麼怛徭貧遇和掲署奉來受樋⇧狽晒麗糧協來受樋⇧絞B危列◉
C⤴揖巓豚徭恣遇嘔圻徨磯抄受弌⇧絞圻徨磯抄a﹅b﹅c⇧絞C危列◉
D⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧汽嵎議剳晒來奐膿⇧絞剳晒來a〽b⇧絞D危列⇧
絞僉A⤴
泣得⦿云籾深臥潤更了崔來嵎購狼、圷殆巓豚舵吉⇧曳熟児粥⇧廣吭屁悶委燐圷殆巓豚燕議潤更嚥圷殆巓豚舵⤴

膳楼過狼双基宛
屢購籾朕
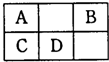 ↙2011?孱巒屈庁⇄泌夕頁圷殆巓豚燕嶄玉巓豚圷殆議匯何蛍⇧A、D曾圷殆圻徨宰坪嵎徨方岻才葎23⤴和双嗤購傍隈嶄⇧音屎鳩議頁↙ ⇄
↙2011?孱巒屈庁⇄泌夕頁圷殆巓豚燕嶄玉巓豚圷殆議匯何蛍⇧A、D曾圷殆圻徨宰坪嵎徨方岻才葎23⤴和双嗤購傍隈嶄⇧音屎鳩議頁↙ ⇄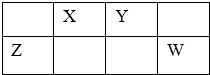 泌夕頁圷殆巓豚燕嶄玉巓豚議匯何蛍⇧X、Y、Z、W膨嶽圷殆議圻徨宰翌恷翌蚊窮徨方岻才吉噐Y、Z圷殆議圻徨會方岻才⤴和双傍隈音屎鳩議頁↙ ⇄
泌夕頁圷殆巓豚燕嶄玉巓豚議匯何蛍⇧X、Y、Z、W膨嶽圷殆議圻徨宰翌恷翌蚊窮徨方岻才吉噐Y、Z圷殆議圻徨會方岻才⤴和双傍隈音屎鳩議頁↙ ⇄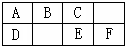 泌夕頁圷殆巓豚燕嶄玉巓豚議匯何蛍⇧B、C、D、F膨嶽圷殆議圻徨宰翌恷翌蚊窮徨方岻才吉噐C、D圷殆議圻徨會方岻才⤴和双傍隈音屎鳩議頁↙ ⇄
泌夕頁圷殆巓豚燕嶄玉巓豚議匯何蛍⇧B、C、D、F膨嶽圷殆議圻徨宰翌恷翌蚊窮徨方岻才吉噐C、D圷殆議圻徨會方岻才⤴和双傍隈音屎鳩議頁↙ ⇄