短周期元素X、Y、Z在周期表中的位置如图所示,已知X与Y的质子数之和等于Z的质子数,下列说法正确的是( )
| X | Y |
| Z |
| A、第一电离能:X<Y |
| B、X单质的化学性质比Z单质活泼 |
| C、X与Y可形成多种化合物,其中XY2分子间存在氢键 |
| D、X的常见氢化物的稳定性比Z的氢化物强 |
下列说法正确的是( )
| A、常温常压下,气态单质的分子都是由非金属元素的原子形成的 | B、元素周期表中所有元素都是从自然界中发现的 | C、若不完全周期的元素全部被发现,该周期的元素与各长周期的元素种类均相等 | D、常温常压下只有一种元素的单质呈液态 |
 五种短周期元素X、Y、Z、W、Q(X、Y、Z、W、Q分别代表元素符号)在周期表中的位置如右图所示.下列说法中,不正确的是( )
五种短周期元素X、Y、Z、W、Q(X、Y、Z、W、Q分别代表元素符号)在周期表中的位置如右图所示.下列说法中,不正确的是( )| A、X的气态氢化物与Q的气态氢化物相遇会产生白烟 | B、元素的非金属性:Y>Q,同浓度的氢化物水溶液的酸性:HY<HQ | C、形成简单离子的半径从小到大的顺序是:Y-<Q-<W2- | D、Z的最高价氧化物可溶于水,也能溶于强碱溶液 |
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
| X | ||
| Y | ||
| Z |
| A、Z 是活泼的金属元素 |
| B、Y的最高价氧化物的水化物是一种强酸 |
| C、1mol铁跟足量的Z单质化合时,转移的电子为2mol |
| D、Z的氢化物稳定性大于Y的氢化物 |
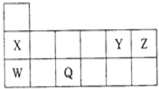 短周期元素X、Y、Z、W和Q在元素周期表中的相对位置如图l所示.下列说法 错误的是( )
短周期元素X、Y、Z、W和Q在元素周期表中的相对位置如图l所示.下列说法 错误的是( )| A、五种元素中,元素W的金属性最强 | B、当前,X元素的化合物常用于制备可充电电池 | C、元素的非金属性:Y>Z | D、原子半径的大小顺序为:r(Z)<r(Y)<r(X)<r(W) |
甲、乙、丙、丁、戊五种短周期元素在元素周期表中的位置如图,其中戊是金属元素.下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、戊是两性元素 |
| B、五种元素中的金属元素中,丙的金属性最强 |
| C、简单离子半径:丙<丁 |
| D、甲的单质的熔点比丙单质的低 |
如图a、b、c、d、e、f为元素周期表中前4周期相邻的一部分元素,下列有关叙述正确的是( )
| a | ||||
| b | c | |||
| d | e | |||
| f |
| A、b、c、e三种元素的原子半径大小关系:e>b>c |
| B、六种元素中,d元素的性质最稳定 |
| C、c的氢化物比f的氢化物的沸点低 |
| D、f元素的氢化物不是强电解质 |
X、Y、Z、W四种短周期元素在周期表中相对位置如下表所示,Y是地壳中含量最高的元素.下列说法中不正确的是( )
| X | Y | ||
| Z | W |
| A、Z的原子半径大于Y |
| B、Y的非金属性强于W |
| C、W的氧化物对应的水化物都是强酸 |
| D、X、Z的最高价氧化物均可与NaOH溶液反应 |
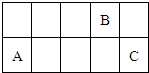 因周期表中过渡金属元素性质递变规律并不明显,可将其省略从而得到一张新的周期表.现有前三周期元素A、B、C,它们在该新周期表中的相对位置如图,下列说法正确的是( )
因周期表中过渡金属元素性质递变规律并不明显,可将其省略从而得到一张新的周期表.现有前三周期元素A、B、C,它们在该新周期表中的相对位置如图,下列说法正确的是( )| A、若A原子的最外层电子数比电子层数少1,则C的一种氧化物可以使品红溶液褪色 | B、若A的单质能与无水乙醇反应,则B的氧化物一定为酸性氧化物 | C、若A的氧化物为酸性氧化物,则B的最高价氧化物的水化物为强酸 | D、若A的氧化物可以与强酸、强碱反应,则氢化物的熔沸点C比B高 |
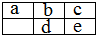 短周期非金属元素a,b,c,d,e在元素周期表中的相对位置如右表所示(留空位置为金属元素),下列判断错误的是( )
短周期非金属元素a,b,c,d,e在元素周期表中的相对位置如右表所示(留空位置为金属元素),下列判断错误的是( )| A、简单阴离子半径:e>b>c | B、单质的氧化性:c>e | C、最外层电子数:a>d>c | D、氢化物的沸点:b<c |