 很多国家已停止使用含铊的杀虫剂.元素周期表中铊的数据见右图,下列说法正确的是( )
很多国家已停止使用含铊的杀虫剂.元素周期表中铊的数据见右图,下列说法正确的是( )| A、TI元素是一种主族元素 | B、TI元素的相对原子质量是204 | C、铊元素的质量数是204.4 | D、TI原子最外层有3个能量相同的电子 |
R、W、X、Y、Z五种短周期元素在周期表的位置如下表.Z原子最外层电子数等于其电子层数.下列说法正确的是( )
| R | W | |||
| X | Y | Z |
| A、R元素最高价氧化物对应水化物的化学式为H2RO4 |
| B、W的气态氢化物的水溶液显弱酸性 |
| C、原子半径由大到小的顺序为X>Y>Z>R>W |
| D、X、R两种元素的氧化物中化学键类型完全相同 |
下列说法正确的是( )
| A、第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | B、第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 | C、同周期非金属氧化物对应水化物的酸性从左到右依次增强 | D、第二周期元素随族序数的递增其最高化合价也递增 |
 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( )| A、原子半径Z<M | B、Y的最高价氧化物对应水化物的酸性比X的弱 | C、非金属性:X<Z | D、M元素最高价氧化物对应水化物具有两性 |
依据元素周期律,下列推断中正确的是( )
| A、酸性:H2SiO3>H2CO3 | B、热稳定性:H2Se>H2S>H2O | C、碱性:CsOH>Ca(OH)2 | D、若离子半径:R2->M+,则原子序数:R>M |
X、Y、Z、W四种元素在元素周期表中的相对位置如图所示,其中X、W的质子数之和为21,由此可知( )
| X | Y | ||
| Z | W |
| A、X位于元素周期表中第2周期、第ⅤA族 |
| B、Y的氢化物(H2Y)不稳定,100℃以上即可分解 |
| C、Z的最高价氧化物的水化物是一种强碱 |
| D、W的非金属性比Y的非金属性弱 |
如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )

| A、气态氢化物稳定性:R>Q | B、元素T的离子结构示意图为 | C、与w同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | D、Q可形成多种含氧酸 |
 短周期元素R、W、X、Y、Z在元素周期表中的相对位置如图所示.下列说法中正确的是( )
短周期元素R、W、X、Y、Z在元素周期表中的相对位置如图所示.下列说法中正确的是( )| A、若X、Y能形成XY2、XY3两种常见化合物,则X、Z的单 质及ZX2均可作为水的消毒剂 | B、若X与Y的最高正化合价和最低负化合价均相同,则W的单质与X和Z的最高价氧化物的水化物均能发生反应 | C、X、Z的氧化物均可能具有两性 | D、五种元素的最高价氧化物的水化物中最多能有3种强酸 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )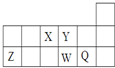

| A、离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+) | B、若存在简单阴离子R2-,则R不一定与Y、W同主族 | C、元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 | D、X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如图所示,下列说法一定正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如图所示,下列说法一定正确的是( )| A、最高价氧化物对应水化物的酸性最强的是W | B、Y与Z只能形成一种化合物 | C、简单阴离子还原性:Y>W | D、Z与Q形成的化合物水溶液可能显酸性 |