题目内容
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )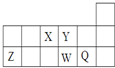

| A、离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+) | B、若存在简单阴离子R2-,则R不一定与Y、W同主族 | C、元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 | D、X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
分析:由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置可知,X为N、Y为O、Z为Al、W为S、Q为Cl,
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大;
B.存在简单阴离子R2-,则R处于ⅥA族;
C.元素X的氢化物与Q的氢化物化合的产物是氯化铵,含有离子键、共价键;
D.X、W、Q元素的最高价氧化物对应水化物分别为硝酸、硫酸、高氯酸,能与碱反应,Z元素的最高价氧化物对应水化物为氢氧化铝,属于两性氢氧化物.
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大;
B.存在简单阴离子R2-,则R处于ⅥA族;
C.元素X的氢化物与Q的氢化物化合的产物是氯化铵,含有离子键、共价键;
D.X、W、Q元素的最高价氧化物对应水化物分别为硝酸、硫酸、高氯酸,能与碱反应,Z元素的最高价氧化物对应水化物为氢氧化铝,属于两性氢氧化物.
解答:解:由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置可知,X为N、Y为O、Z为Al、W为S、Q为Cl,
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径r(S2-)>r(Cl-)>r(O2-)>r(Al3+),故A正确;
B.若存在简单阴离子R2-,则R处于ⅥA族,一定与Y、W同主族,故B错误;
C.元素X的氢化物与Q的氢化物化合的产物是氯化铵,含有离子键、共价键,故C正确;
D.X、W、Q元素的最高价氧化物对应水化物分别为硝酸、硫酸、高氯酸,能与碱反应发生中和反应,Z元素的最高价氧化物对应水化物为氢氧化铝,属于两性氢氧化物,能与强碱反应,故D正确,
故选B.
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径r(S2-)>r(Cl-)>r(O2-)>r(Al3+),故A正确;
B.若存在简单阴离子R2-,则R处于ⅥA族,一定与Y、W同主族,故B错误;
C.元素X的氢化物与Q的氢化物化合的产物是氯化铵,含有离子键、共价键,故C正确;
D.X、W、Q元素的最高价氧化物对应水化物分别为硝酸、硫酸、高氯酸,能与碱反应发生中和反应,Z元素的最高价氧化物对应水化物为氢氧化铝,属于两性氢氧化物,能与强碱反应,故D正确,
故选B.
点评:本题考查元素周期表与元素周期律,难度不大,注意理解掌握离子半径的比较规律.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
碱金属元素可形成离子型氢化物,下表是同一短周期元素X、Y、Z三种元素氢化物的某些性质
则这三种元素的原子序数从大到小的排列顺序为( )
| 元素 | 熔点(℃) | 沸点(℃) | 与水作用 | 纯液体的导电性 |
| X | -183 | -162 | 不与水反应也不溶于水 | 不导电 |
| Y | -102 | 19 | 放热,形成的酸是弱酸 | 不导电 |
| Z | 680 | - | 剧烈反应生成H2,溶液呈碱性 | 导电 |
| A、X、Y、Z |
| B、Z、X、Y |
| C、Y、X、Z |
| D、Z、Y、X |
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法中不正确的是( )
| X | Y | ||||
| Z | M | R | |||
| A、元素X和Y可以形成两种以上的气态化合物 |
| B、原子半径的大小顺序为:r(Z)>r(M)>r(R) |
| C、元素的最高价氧化物对应水化物的酸性R强于M |
| D、加热蒸干由元素R和Z形成的化合物的水溶液可以得到该化合物的晶体 |
 短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )