题目内容
 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如图所示,下列说法一定正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如图所示,下列说法一定正确的是( )| A、最高价氧化物对应水化物的酸性最强的是W | B、Y与Z只能形成一种化合物 | C、简单阴离子还原性:Y>W | D、Z与Q形成的化合物水溶液可能显酸性 |
分析:短周期主族元素.其中只有Z是金属,W的单质是黄色固体,则W为S,由X、Y、W在周期表中的相对位置可知,Y为O,X为C,X、Y、Z、W、Q是原子序数依次增大,所以Q为Cl,而Z可能为Na、Mg、Al中的一种,然后结合元素的单质及化合物的性质来解答.
解答:解:短周期主族元素.其中只有Z是金属,W的单质是黄色固体,则W为S,由X、Y、W在周期表中的相对位置可知,Y为O,X为C,X、Y、Z、W、Q是原子序数依次增大,所以Q为Cl,而Z可能为Na、Mg、Al中的一种,
A、最高价氧化物对应水化物的酸性最强的是Cl,Q元素,故A错误;
B、Z可能为Na、Mg、Al中的一种,若Z为Na与O可以形成两种氧化物,故B错误;
C、S2-的还原性强于O2-,即还原性W2->Y2-,简单阴离子还原性:Y<W,故C错误;
D.若Z为Na,则Z与Q形成的化合物NaCl的水溶液为中性,若Z为Al,Z与Q形成的化合物AlCl3水溶液为酸性,故D正确;
故选:D
A、最高价氧化物对应水化物的酸性最强的是Cl,Q元素,故A错误;
B、Z可能为Na、Mg、Al中的一种,若Z为Na与O可以形成两种氧化物,故B错误;
C、S2-的还原性强于O2-,即还原性W2->Y2-,简单阴离子还原性:Y<W,故C错误;
D.若Z为Na,则Z与Q形成的化合物NaCl的水溶液为中性,若Z为Al,Z与Q形成的化合物AlCl3水溶液为酸性,故D正确;
故选:D
点评:本题考查位置、结构、性质,注意把握元素周期表和元素周期律,元素的推断是解答本题的关键,W为淡黄色固体为突破口,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
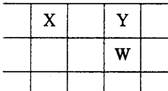 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )| A、五种元素中,原子半径最大的是W | B、Y与Z形成的化合物都可以和盐酸反应 | C、Y的简单阴离子比W的简单阴离子还原性强 | D、Z与Q形成的化合物水溶液一定显酸性 |
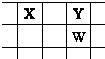 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )| A、五种元素中,原子半径最大的是W | B、Y的简单阴离子比W的简单阴离子还原性强 | C、Y与Z形成的化合物都可以和盐酸反应 | D、Z与Q形成的化合物水溶液一定显酸性 |