为探究铁和稀硝酸反应后溶液中铁元素存在形式,某化学实验兴趣小组设计实验如下:
提出假设:
假设1:溶液中只有Fe2+;
假设2: ;
假设3: .
设计实验方案、验证假设:(请完成下列表格)
问题分析:
(1)若已知铁和稀硝酸反应生成标准状况下NO气体2.24L,则上述反应中参加反应的硝酸物质的量为 ;
(2)若假设1正确,请写出铁和稀硝酸发生该反应的离子方程式: ;
(3)某同学向反应后溶液中滴加适量NaOH溶液,未发现白色沉淀产生,由此断定溶液中没有Fe2+,他这种说法对吗?请分析理由: .
提出假设:
假设1:溶液中只有Fe2+;
假设2:
假设3:
设计实验方案、验证假设:(请完成下列表格)
| 实验操作 | 预期现象与结论 |
| 1. |
若溶液不变红,则假设1正确; 若溶液变红,则假设2或假设3正确 |
| 2.另取少许反应后溶液于试管中,滴加1-2滴0.01mol/L KMnO4溶液,振荡 |
(1)若已知铁和稀硝酸反应生成标准状况下NO气体2.24L,则上述反应中参加反应的硝酸物质的量为
(2)若假设1正确,请写出铁和稀硝酸发生该反应的离子方程式:
(3)某同学向反应后溶液中滴加适量NaOH溶液,未发现白色沉淀产生,由此断定溶液中没有Fe2+,他这种说法对吗?请分析理由:
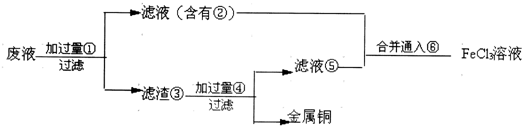
(1)有一瓶存放时间较长的硫酸亚铁,外观上并无明显变化,但某学生怀疑其有部分因氧化而变质,请你设计1个检验硫酸亚铁是否变质的实验方案: .如果有变质,当配制硫酸亚铁溶液时,应如何除去变质的杂质? .
(2)FeCl3溶液棕黄色,对此溶液,分别做如下实验,请填表:
(2)FeCl3溶液棕黄色,对此溶液,分别做如下实验,请填表:
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量 铁粉 |
||
| ② | 加入少量Na2O2粉末 | ||
| ③ | 加入少量AgNO3溶液 |
下列各组物质中,滴入KSCN溶液显红色的是 ( )
| A、过量铜粉和硫酸铁溶液 | B、过量铁粉与稀硫酸 | C、少量的铁粉与盐酸 | D、氯水与氯化亚铁溶液 |
下列实验中,能观察到明显变化现象的是( )
| A、把KSCN溶液滴入FeCl3溶液中 | B、把铁片放入冷的浓硫酸中 | C、把盐酸滴入氢氧化钾溶液中 | D、把淀粉溶液滴入KI溶液中 |
下列各组物质反应后,滴入KSCN溶液,显红色的是( )
| A、过量的铁与稀盐酸反应 | B、过量的铁粉与氯化铜溶液反应 | C、过量氯水与氯化亚铁溶液反应 | D、过量铁粉与三氯化铁溶液反应 |
某矿石样品中可能含铁,为确定其成分,进行如下操作:下列有关说法正确的是( )


| A、向溶液乙中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | B、向溶液甲中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | C、向溶液乙中滴加少量氢氧化钠溶液,一定出现红褐色沉淀 | D、该矿石一定为赤铁矿 |
下列操作可以达到实验目的是( )
| A、要证明某溶液中不含Fe3+而可能含Fe2+,先加氯水,再加少量的KSCN溶液 | B、为防止FeSO4被氧化而变质,常在溶液中加入少量的铁粉 | C、将Fe(OH)2露置在空气中加热灼烧可以得到FeO | D、向AlCl3溶液中加入过量氨水,过滤,沉淀灼烧可得到Al2O3 |
要想证明某溶液中是否含有Fe3+,下列操作中正确的是( )
| A、加入铁粉 | B、滴加KSCN溶液 | C、通入氯气 | D、加入铜片 |
将一定量的铁片和浓硫酸混合加热,充分应后得到溶液X,X中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,应选用( )
| A、KSCN溶液和氯水 | B、铁粉和KSCN溶液 | C、浓氨水 | D、酸性KMnO4溶液 |