类比推断是学习化学的一种重要方法,下列推断正确的是( )
| A、HF和NH3的水溶液都能导电,所以均为电解质 | B、SO2和NO2都能与水反应生成酸,所以均为酸性氧化物 | C、电解熔融NaCl制取Na,所以电解熔融MgCl2也能制取Mg | D、Na2O和Na2O2所含元素相同,所以与CO2反应的产物相同 |
取100mL 18.3mol/L的H2SO4与Zn反应,当Zn完全溶解时,生成气体在标况下占有的体积为22.4L,将所得的溶液稀释成1L,测得溶液的H+浓度为1mol/L,则所生成的气体中SO2与H2的体积比约为( )
| A、1:2 | B、2:1 | C、1:4 | D、4:1 |
 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )| A、线段AB代表Fe2+物质的量的变化情况 | B、原混合溶液中 c(FeBr2)=6mol/L | C、DE段的离子反应可表示为2Br-+Cl2=Br2+2Cl- | D、原溶液中n(Fe2+):n(I-):n(Br-)=2:2:3 |
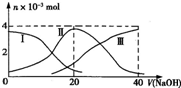 常温下,向20mL 0.2mol?L-1 H2SO3,溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒的物质的量变化曲线如图所示.(其中I代表H2SO3、Ⅱ代表HS
常温下,向20mL 0.2mol?L-1 H2SO3,溶液中滴加0.2mol?L-1 NaOH溶液.有关微粒的物质的量变化曲线如图所示.(其中I代表H2SO3、Ⅱ代表HS| O | - 3 |
| O | 2- 3 |
| A、当V(NaOH)=0时,由水电离出的c(H+)=1.0×10-12?? | ||||
B、当V(NaOH)=20 mL时:c(Na+)>c(HS
| ||||
C、当V(NaOH)=40 mL时2c(Na+)=c(S
| ||||
| D、当V(NaOH)=40 mL后,继续滴加NaOH溶液,溶液的温度会继续升高 |
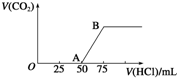 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )A、OA段所发生反应的离子方程式:H++OH-═H2O;CO32-+H+═HCO
| ||
| B、NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1 | ||
| C、产生的CO2体积(标准状况下)为0.056 L | ||
| D、原NaOH溶液的物质的量浓度为0.5 mol?L-1 |
现有Na2CO3、H2SO4、Ba(OH)2三种物质的量浓度与体积都相等的溶液,若以不同顺序将它们中的两种混合起来,出现沉淀后过滤,再将滤液与第三种溶液混合起来,最终所得的溶液( )
| A、一定呈酸性 | B、不可能呈碱性 | C、可能呈中性 | D、一定呈中性 |
有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液,若将甲蒸发掉一半水分,在乙中通入少量的CO2,丙不变,然后分别向甲、乙、丙三瓶中加入同浓度的盐酸,完全反应后所需盐酸溶液的体积是( )
| A、甲=乙=丙 | B、丙>乙>甲 | C、乙>甲=丙 | D、甲=丙>乙 |
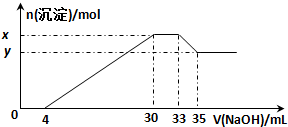 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
| A、x与y的差值为0.01 mol | B、原溶液中c(Cl-)=0.75 mol?L-1 | C、原溶液的pH=1 | D、原溶液中n(Mg2+):n(Al3+)=5:2 |
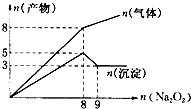 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )| A、2 mol、3 mol、8 mol | B、3 mol、2 mol、8 mol | C、2 mol、3 mol、4 mol | D、3 mol、2 mol、4 mol |



