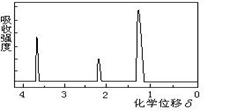
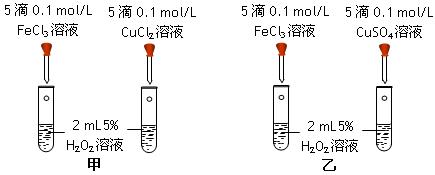
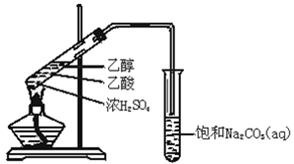
(16分)有一种催化剂为铁的常见的氧化物,为探究该氧化物的成分:
(一)某同学将适量稀硝酸加入少许样品中加热溶解;取少许所得溶液,滴加KSCN溶液,出现红色,由此得出该氧化物中铁元素为+3价,你认为该结论 (合理或不合理),理由: 。
(二)请你完成对该铁的氧化物成分的探究分析:
提出对该氧化物的合理假设:
a.假设1: ;b.假设2:假设该氧化物为FeO;c.假设3: 。
(三)[设计方案证明上述假设,选择合适的仪器和药品]
(四)[实验过程以及结论分析]:(请填写空格①和②)
| 实验操作 | 预期现象与结论 |
| 步骤1:用滴管取一定量3mol·L-1H2SO4于试管中,加热煮沸数分钟除去溶于其中的氧气 |  |
| 步骤2:用药匙取少量样品于试管中,用滴管加入适量除去氧气的3mol·L-1H2SO4并加热,充分反应得A溶液 | 固体溶解,溶液颜色有变化 |
| 步骤3:取少许A溶液于试管中,滴加1—2滴20%KSCN溶液,振荡 | ① |
| 步骤4:另取少许A溶液于试管中,滴加1—2滴0.2mol·L-1KMnO4溶液,振荡 | ② |

 6CuFeS2+19O2
6CuFeS2+19O2 6CuO+2Fe3O4+12SO2
6CuO+2Fe3O4+12SO2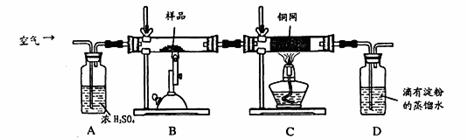
 气充分反应 b.除去空气中的水份
气充分反应 b.除去空气中的水份 +H2O=H2SO4+2HI,达到终点时消耗I2溶液20.00mL,判断滴定达到终点的现象为 ,通过计算,该黄铜矿的纯度为 (Cu:64 Fe:56 S:32)
+H2O=H2SO4+2HI,达到终点时消耗I2溶液20.00mL,判断滴定达到终点的现象为 ,通过计算,该黄铜矿的纯度为 (Cu:64 Fe:56 S:32)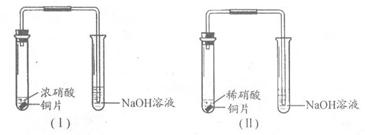
 (一)甲组:实验方案:镁铝合金
(一)甲组:实验方案:镁铝合金 测定剩余固体质量
测定剩余固体质量 盘天平称量一定质量镁铝合金粉末
盘天平称量一定质量镁铝合金粉末 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积

 并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
并最终得到固体物质1.45g。则该合金中铝的质量分数为 。


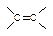 +IBr →
+IBr →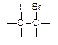 ②IBr+KI=I2+KBr ③I2+2S2O32-=2I-+S4O62-
②IBr+KI=I2+KBr ③I2+2S2O32-=2I-+S4O62-
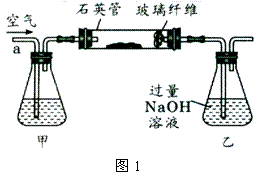
 g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:
g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为: 。
。
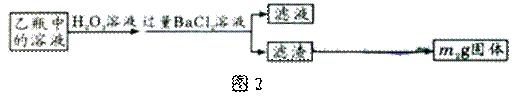

 ;
;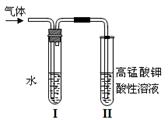
 先通入水中?填“是”或”否”
先通入水中?填“是”或”否”  。
。