 某化学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,并设计如下实验方案进行探究.
某化学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,并设计如下实验方案进行探究.
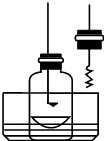
步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、胶塞等装配如图所示的装置.另准备一只胶塞,其中有一根铜丝穿过,铜丝末端固定一根镁条备用.
步骤2:引燃燃烧匙中的试剂,塞好瓶塞.燃烧结束后,调节广口瓶内外液面相平.
步骤3:点燃镁条,更换胶塞,镁条继续燃烧,反应结束后,广口瓶内水面上升.
步骤4:取蒸发皿中得到的固体,加盐酸溶解.向溶液中加入过量氢氧化钠溶液,有白色沉淀生成,同时得到一种能使湿润红色石蕊试纸变蓝的气体.
(1)为除去广口瓶中的氧气,燃烧匙中最好应装入下列试剂中的(填序号)______.A.炭粉 B.铁粉 C.红磷
(2)“步骤2”中调节内外液面相平的方法:______
(3)写出Mg3N2溶于足量盐酸生成两种氯化物的化学方程式:______.
(4)某同学直接将镁条在空气中点燃,并将所得白色固体进行“步骤4”的实验,结果无气体生成,其原因是______.
(5)兴趣小组同学为比较镁和铝的金属性强弱,设计了下表中的实验方案一,请你再设计一种不同的实验方案.实验试剂和用品:镁条、铝条、0.1mol?L-1MgCl2溶液、0.1mol?L-1AlCl3溶液、0.1mol?L-1HCl溶液、0.1mol?L-1NaOH 溶液、pH 试纸(其他实验仪器可任选)
| 实验操作 | 实验现象 | |
| 方案一 | 取已除去表面氧化膜的镁条和铝条, 分别和0.1mol?L-1HCl溶液反应 | 均有气泡产生,镁条反应 比铝条反应更剧烈 |
| 方案二 |
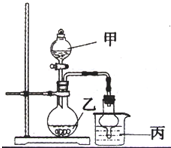 如图所示实验装置进行实验(必要时可以进行加热),下列实验现象描述不正确的是
如图所示实验装置进行实验(必要时可以进行加热),下列实验现象描述不正确的是
| 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | H2O2 | MnO2 | FeCl2 | 溶液由浅绿色变为棕黄色 |
| B | 浓氨水 | CaO | AgNO3 | 开始有白色沉淀生成,随后白色沉淀减少以至完全消失 |
| C | H2SO4 | Na2SO3 | BaCl2 | 产生白色沉淀 |
| D | 浓HNO3 | Cu | NaHCO3 | 有无色气体生成 |
- A.A
- B.B
- C.C
- D.D
 氯化铵是一种重要的化工原料,应用广泛.
氯化铵是一种重要的化工原料,应用广泛. NaCl+N2↑+2H2O
NaCl+N2↑+2H2O 、H+、S2-、MnO
、H+、S2-、MnO 、Fe3+、[Al(OH)4]-、CO
、Fe3+、[Al(OH)4]-、CO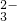 、NH
、NH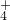 、SO
、SO 、OH-.已知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子可能是
、OH-.已知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子可能是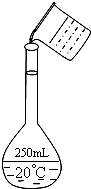 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有: