氯化铜晶体中常含FeCl2杂质,为制得纯净氯化铜晶体(CuCl2?2H2O),首先将其溶于稀盐酸中,然后按下面所示操作步骤进行提纯.
| 氢氧化物开始沉淀时的pH | 氯氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
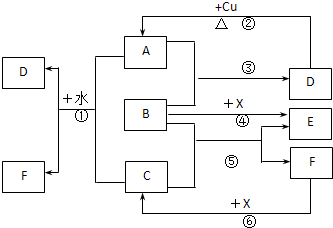
已知:(1)下列物质中,最适合作为氧化剂X的是______(填序号)
A.H2O2 B.KMnO4 C.NaClO D.浓硫酸
写出加入X后发生反应离子的方程式______.
(2)加入的物质Y可以是______,目的是______
(3)某同学利用反应Cu+2H+ Cu2++H2↑设计实验来
制取氯化铜溶液.该同学设计的装置应该为______(填“原电池”或“电解池”).请画出该同学设计的装置图,并指明电极材料和电解质溶液.
(4)从CuCl2稀溶液中得到CuCl2?2H2O晶体,在蒸发结晶的过程中,为了防止Cu2+的水解,应采取的措施是______.
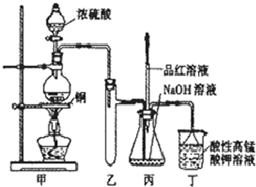 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4 是否剩余______,原因是______
(2)向反应后的溶液中加入足量的CuO,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O)某小组同学采用加热法测定该晶体里结晶水 x 的值;
①在他们的每次实验操作中至少称量______次.
③加热法测定该晶体里结晶水 x 的值,结晶水完全失去的判断方法是______;
④下面是三次实验数据的平均值
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
(3)下列说法正确的是:______(填序号).
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶;
b.KMnO4溶液用于尾气处理;
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生;
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3;
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3.