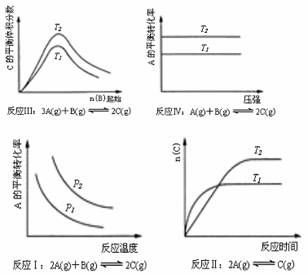
(12分) 设反应①![]() 的平衡常数为
的平衡常数为![]() 。反应②
。反应②![]() 的平衡常数为
的平衡常数为![]() ,在不同温度下,
,在不同温度下,![]() 、
、![]() 的值如下:
的值如下:
| 温度 |
|
|
|
| 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(1)从上表可以推断:反应①是_______________ (填“吸”、“放”)热反应。
(2)现有反应③![]() 写出该反应的平衡常数K3的数学表达
写出该反应的平衡常数K3的数学表达
式:K![]() =____________。
=____________。
(3)根据反应①与②,可推导出K![]() 、K
、K![]() 与K
与K![]() 之间的关系式_______________。据
之间的关系式_______________。据
![]() 此关系式及上表数据,也能推断出反应③是“吸热”还是“放热”反应。问:要使反应
此关系式及上表数据,也能推断出反应③是“吸热”还是“放热”反应。问:要使反应
③在一定条件下建立的平衡向正反应方向移动,可采取的措施有___________________
(填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
(4)图l、2表示该反应③在时刻t![]() 达到平衡、在时刻t
达到平衡、在时刻t![]() 分别因改变某个条件而发生变化的
分别因改变某个条件而发生变化的
情况:
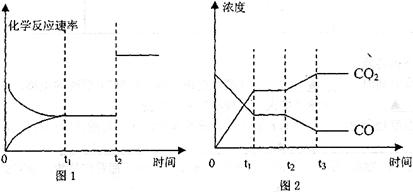
①图l中时刻t![]() 发生改变的条件是________________________________________
发生改变的条件是________________________________________
②图2中时刻t![]() 发生改变的条件是________________________________________
发生改变的条件是________________________________________
(12分)在密闭容器中,保持一定温度进行如下反应N2(g)+3H2(g)![]() 2NH3(g), 已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
2NH3(g), 已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=___________。
(2)平衡常数K值越大,表明建立平衡时___________(填字母序号)。
A.N2的转化率越高 B.NH3的产量越大
C.正反应进行得越彻底 D.化学反应速度越快
(3)a与b的关系是:a b(填>、<、=)
(4)填写下表:
| 状态 条件 | 起始时物质的物质的量(mol) | 平衡时NH3的物质的量 (mol) | |||
| 编号 | X(N2) | Y(H2) | Z(NH3) | ||
| 恒容 | ① | 1 | 3 | 0 | b |
| ② | 0 | 0 | b | ||
| ③ | 2.25 | b | |||